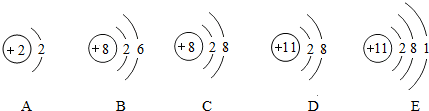
4.纳米级Cu
2O具有优良的催化性能.某兴趣小组对它开展了以下系列研究.
Ⅰ、纳米级Cu
2O的用途研究
【查阅资料】
①氨气是一种有刺激性气味的气体,在高浓度氧气中才能燃烧,生成氮气和水4NH
3+3O
2═2N
2+6H
2O.
②在纳米级Cu
2O的催化下,氨气与氧气在一定温度下还可以同时发生以下化学反应:4NH
3+5O
2═4NO+6H
2O,工业上用NO制备硝酸、氮肥等化工产品.
【实验1】
用图1所示的实验装置验证氨气在氧气中燃烧时现象如图.实验时要将过量的氧气从进气口a(填“a”或“b”)通入,并在b(填“a”或“b”)管上端点燃氨气.另外,实验时需“先通入氧气,后通入氨气”,其理由是NH
3的燃烧需要高浓度氧气,先通氧气可以保证氨气被点燃.
【实验2】
用图2所示的实验装置研究“在纳米级Cu
2O催化作用下,氨气与氧气的化学反应,并对生成物进行成分分析”.根据所得的气体成分数据,同学们绘制了曲线图(见图3)

发现在纳米级Cu
2O的催化作用下,300℃时以生产氮气为主.若利用后续处理装置模拟硝酸的工业制法,则最好将电热丝的温度控制在900℃左右.
Ⅱ.纳米级Cu
2O的制备研究
利用某些特殊的细菌,在一定条件下将某岩石中的不溶性硫化铜(CuS)转化为可溶性硫化铜,进而制得纳米级Cu
2O,其流程如图:

(1)在细菌作用下,岩石中的硫化铜(CuS)与空气中的氧气反应生成硫酸铜,反应的化学方程式为CuS+2O
2$\frac{\underline{\;细菌\;}}{\;}$CuSO
4.
(2)③中观察到的现象是产生蓝色沉淀.
(3)经测定该岩石由硫化铜(CuS)和其它不含铜元素的物质组成.现用1000g该岩石制得28.8g纯氧化亚铜(Cu
2O),该纯氧化亚铜(Cu
2O)中铜元素的质量是25.6g.若制得氧化亚铜(Cu
2O)的过程中,铜元素的总损耗为20%,通过计算确定该岩石中硫化铜(CuS)的质量分数4.8%(请写出计算过程).



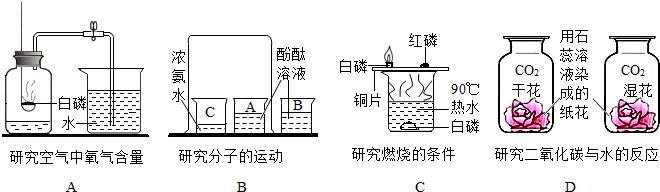
 水是生命之源.
水是生命之源.