
科目: 来源: 题型:解答题
| 猜想一:NaOH | 猜想二:NaOH、Ca(OH)2 |
| 猜想三:NaOH、Na2CO3 | 猜想四:NaOH、Na2CO3、Ca(OH)2 |
| 操作 | 现象 | 结论 |
| ①取少量滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| ②另取少量滤液,向其中滴入足量稀盐酸 | 无明显现象 | 猜想一成立 |
查看答案和解析>>
科目: 来源: 题型:解答题
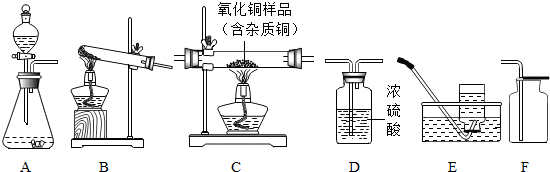
查看答案和解析>>
科目: 来源: 题型:解答题
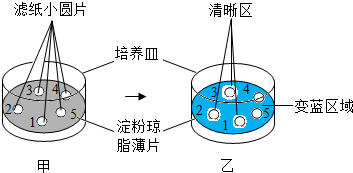 某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:
某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:| 滤纸编号 | 溶液成分 |
| 1 | 淀粉酶溶液 |
| 2 | 淀粉酶溶液-稀盐酸 |
| 3 | 淀粉酶溶液-稀碳酸钠溶液 |
| 4 | 稀盐酸 |
| 5 | 稀碳酸钠溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| OH- | Cl- | CO32- | |
| H+ | / | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不溶 |
| Na+ | 溶 | 溶 | 溶 |
| 实验步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量待测溶液于试管中,向其中滴加足量的稀盐酸 | 有气泡产生 | 猜想(1)不成立,写出有关反应化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
| 步骤二:取少量待测溶液于试管中,然后滴加足量的BaCl2溶液,静置,向上层清液中滴加酚酞 | 有沉淀产生,溶液不变红(或溶液变红) | 猜想(2)或(3)成立,写出有关反应化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 多骑自行车,少开汽车 | B. | 大量植树造林 | ||
| C. | 充分利用太阳能 | D. | 直接燃烧煤炭 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 含氧元素的化合物都属于氧化物 | |
| B. | 稀硫酸能使无色酚酞溶液变红色 | |
| C. | 金刚石和石墨物理性质存在着明显差异,是因为构成它们的原子大小不同 | |
| D. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目: 来源: 题型:解答题
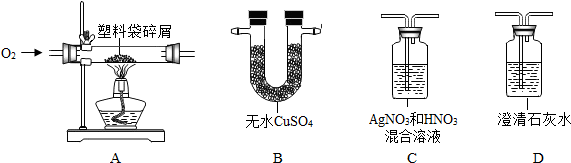
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com