
科目: 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(CO) | 氧气 | 点燃 |
| B | KCl(K2SO4) | 蒸馏水和过量氯化钡溶液 | 溶解、过滤、蒸发 |
| C | NH3(H2O) | 足量的浓硫酸 | 洗气 |
| D | Cu(CuO) | 足量的稀硫酸 | 浸泡、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
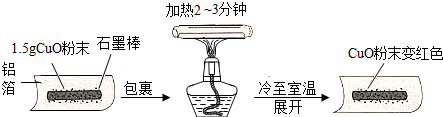
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 燃着的酒精灯不慎碰倒,立即用湿布盖灭 | |
| B. | 检验氢气纯度时,没有听到任何响声,表明氢气已纯净 | |
| C. | 配制100g 10%的氯化钠溶液需要10g 氯化钠和100g 水 | |
| D. | 用pH试纸测定溶液酸碱度时,先将pH试纸用水润湿,然后再测定 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Mg | B. | MgO | C. | Mg(OH)2 | D. | MgCO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
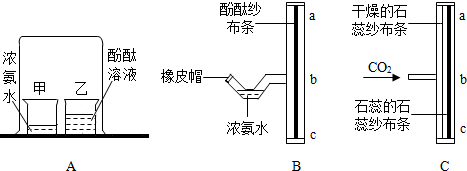
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 制取气体时,连好发生装置后检查其气密性 | |
| B. | 没有腐蚀性的固体药品直接放在托盘上称量 | |
| C. | 测定某种试剂的pH时,将试纸伸入待测液中 | |
| D. | 做实验用剩的药品,要及时放回原试剂瓶中 |
查看答案和解析>>
科目: 来源: 题型:解答题
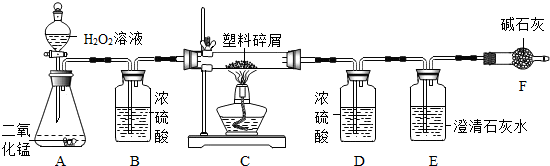
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com