
科目: 来源: 题型:解答题
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 用铂丝蘸取该固体在酒精灯上灼烧. | 火焰呈黄色 | 固体中含有Na+. |
| ② | 将该固体置于足量蒸馏水中. | 固体全部溶解. | 固体可溶于水. |
| ③ | 取少量②所得溶液,向其中滴加紫色石蕊试液,并振荡. | 溶液变蓝. | 溶液为碱性. |
| ④ | (此格不必填写) |
查看答案和解析>>
科目: 来源: 题型:解答题
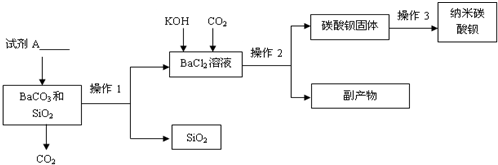
查看答案和解析>>
科目: 来源: 题型:解答题
 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | 没有氢氧化钙 |
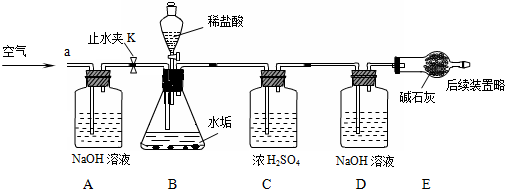
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | M可能是BaO | B. | 相对分子质量:M>N | ||
| C. | N中一定含有氢元素 | D. | N可能是HNO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 相关化学反应方程式 |
| 1除去空气中粉尘、二氧化碳、干燥后,再除去氧气. | 除去氧气的化学反应方程式为2Cu+O2$\frac{\underline{\;高温\;}}{\;}$2CuO; |
| 2用上述制得的氮气通入装有碳和三氧化二铝硬质玻璃管中高温制取氮化铝样品(如图1). | 装置中发生化学反应的化学方程式为 N2+3C+Al2O3 $\frac{\underline{\;高温\;}}{\;}$2AlN+3CO. |
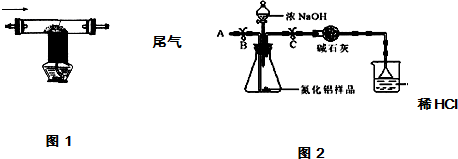
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CaCl2固体(CaCO3):加足量稀硫酸、蒸发、结晶 | |
| B. | NaCl固体(Na2CO3):加足量石灰水、蒸发、结晶 | |
| C. | Fe粉(Cu):加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | MnO2固体(KCl):加足量水溶解、过滤、洗涤、干燥 |
查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题
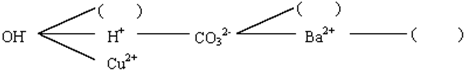
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com