
科目: 来源: 题型:选择题
| A. | 只要功夫深,铁杵磨成针 | B. | 爆竹声中一岁除,春风送暖入屠苏 | ||
| C. | 千锤万凿出深山,烈火焚烧若等闲 | D. | 春蚕到死丝方尽,蜡炬成灰泪始干 |
查看答案和解析>>
科目: 来源: 题型:解答题
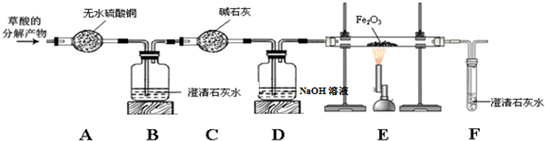
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

| 实验步骤 | 实验现象 | 实验结论 |
| a.取上述无色液体X少量于试管中,至不再冒气泡为止,加入足量的氯化钙溶液. | 产生白色沉淀 | 无色溶液X中含有Na2CO3 |
| b.取步骤a所得上层清液少量,滴加稀盐酸. | 没有气泡产生 | 无色溶液X中不含NaHCO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
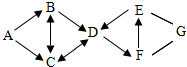 现有A~G 7种初中化学常见物质,其中A是可以治疗胃酸过多的盐,C在常温下为气体,D为大理石主要成分,E在农业上可用于改良酸性土壤,G中含有三种元素.它们的转化关系如图所示(箭头表示一种物质可以转化成另一种物质,横线表示两种物质间能发生反应,部分条件与产物已略去):
现有A~G 7种初中化学常见物质,其中A是可以治疗胃酸过多的盐,C在常温下为气体,D为大理石主要成分,E在农业上可用于改良酸性土壤,G中含有三种元素.它们的转化关系如图所示(箭头表示一种物质可以转化成另一种物质,横线表示两种物质间能发生反应,部分条件与产物已略去):查看答案和解析>>
科目: 来源: 题型:解答题
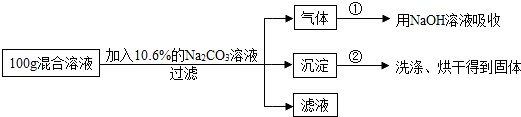
查看答案和解析>>
科目: 来源: 题型:解答题
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 锰 | 铁 |
| 元素符号 | H | C | O | Cl | Mn | Fe |
查看答案和解析>>
科目: 来源: 题型:选择题
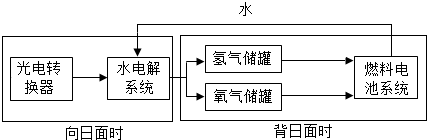
| A. | 燃料电池系统中发生化合反应生成了水 | |
| B. | 燃料电池系统产生的能量实际上来自于太阳能 | |
| C. | 水电解系统中是将电能转化为化学能 | |
| D. | 背日面时氢气燃烧,将化学能转化为光能和热能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com