
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验NaOH中是否含有Na2CO3 | 滴加少量稀盐酸 |
| B | 鉴别NaOH和Ca(OH)2溶液 | 加Na2CO3溶液 |
| C | 清洗铁制品表面的铁锈 | 用水洗涤 |
| D | 除去CO2中的CO | 通入足量的澄清石灰水中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
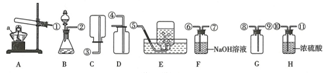
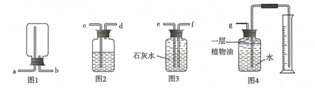
查看答案和解析>>
科目: 来源: 题型:解答题
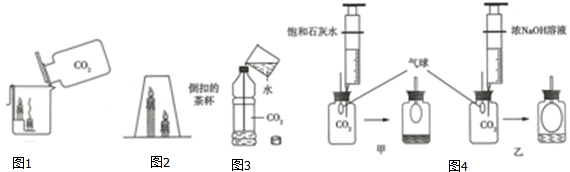
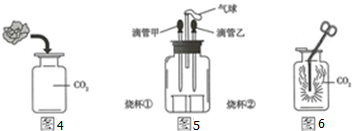
查看答案和解析>>
科目: 来源: 题型:解答题
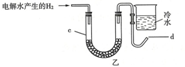 科学家用点燃氢气的,验证燃烧产物的方法,证实了水的组成.
科学家用点燃氢气的,验证燃烧产物的方法,证实了水的组成.查看答案和解析>>
科目: 来源: 题型:解答题
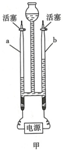 (1)科学家用通电的方法使水分解,从而证明了水的组成.把水注入水电解装置甲中,接通直流电电源后,可以观察到的现象是电极上有气泡生成;一段时间后可以观察到a、b两管中的气体体积比约为2:1;由此可判断与a管相连的一极是电源的负极.
(1)科学家用通电的方法使水分解,从而证明了水的组成.把水注入水电解装置甲中,接通直流电电源后,可以观察到的现象是电极上有气泡生成;一段时间后可以观察到a、b两管中的气体体积比约为2:1;由此可判断与a管相连的一极是电源的负极.查看答案和解析>>
科目: 来源: 题型:填空题
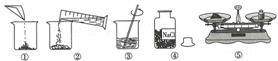
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 红磷在氧气中剧烈燃烧,生成大量白色烟雾 | |
| B. | 硫在空气中燃烧,发出蓝紫色火焰,生成白烟 | |
| C. | 煤炭在空气中燃烧,生成二氧化碳气体 | |
| D. | 生石灰与水反应,放出热量 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
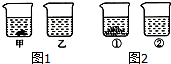
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com