
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CaO+H2O═Ca(OH)2 | B. | HCl+AgNO3═AgCl↓+HNO3 | ||
| C. | 3H2SO4+2Fe(OH)3═Fe2(SO4)3+6H2O | D. | H2SO4+BaCl2═BaSO4↓+2HCl |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
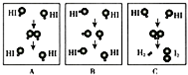 化学反应的多角度认识
化学反应的多角度认识| 实验 | 硫酸(10%)体积/mL | 温度/℃ | 其他物质 |
| I | 2mL | 20 | / |
| Ⅱ | 2mL | 20 | 10滴饱和MnS04溶液 |
| Ⅲ | 2mL | 30 | / |
| Ⅳ | 1mL | 20 | 1mL蒸馏水 |
查看答案和解析>>
科目: 来源: 题型:解答题
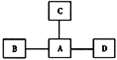 通常将纯净物分成单质、氧化物、酸、碱、盐等类别,从类别的角度来研究它们的性质及反应.
通常将纯净物分成单质、氧化物、酸、碱、盐等类别,从类别的角度来研究它们的性质及反应.| 物质分类 | 单质 | 化合物 | ||
| 元素种类 | 金属 | 非金属 | 两种 | 三种 |
| 物质代号 | A、B | C、D | E、F | G |
查看答案和解析>>
科目: 来源: 题型:解答题
 归纳总结是学习的重要方法,酸、碱、盐之间的反应有着一定的规律.
归纳总结是学习的重要方法,酸、碱、盐之间的反应有着一定的规律.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com