
科目: 来源: 题型:解答题
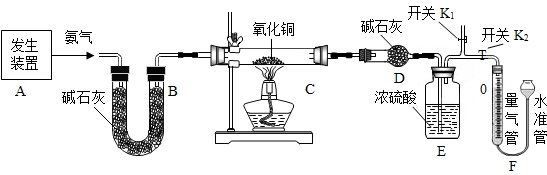
查看答案和解析>>
科目: 来源: 题型:解答题
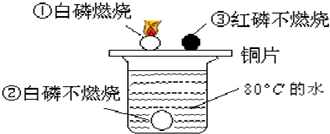
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 泡沫塑料不属于易燃物 | |
| B. | 火灾发生后应用湿毛巾捂住口鼻迅速逃离,并拨打火警119 | |
| C. | 只要达到着火点,可燃物一定会燃烧 | |
| D. | 可燃物燃烧的同时一定还会发生爆炸 |
查看答案和解析>>
科目: 来源: 题型:解答题
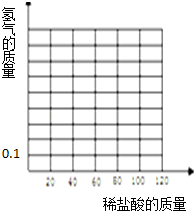 某同学为了测试一段表面被氧化的镁条的纯度.取11.6g该镁条于烧杯中,向烧杯中分五次加入等质量的同种稀盐酸,实验过程中得到的数据如下:
某同学为了测试一段表面被氧化的镁条的纯度.取11.6g该镁条于烧杯中,向烧杯中分五次加入等质量的同种稀盐酸,实验过程中得到的数据如下:| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量 | 20g | 20g | 20g | 20g | 20g |
| 产生氢气的质量 | 0.1g | 0.2g | 0.2g | mg | 0.1g |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
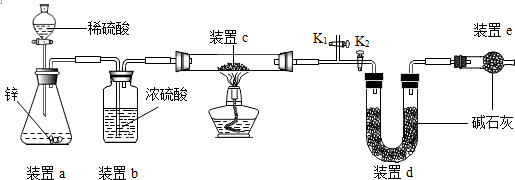
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
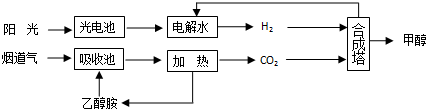
查看答案和解析>>
科目: 来源: 题型:解答题
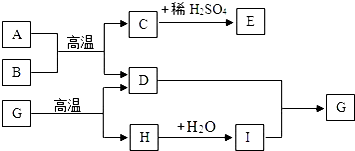 A~J是初中化学中常见的物质,其中A为一种化合物气体,B为红棕色固体,E为浅绿色溶液,H是一种食品干燥剂,它们之间的关系如下图(部分反应物或生成物已略去).
A~J是初中化学中常见的物质,其中A为一种化合物气体,B为红棕色固体,E为浅绿色溶液,H是一种食品干燥剂,它们之间的关系如下图(部分反应物或生成物已略去).查看答案和解析>>
科目: 来源: 题型:解答题
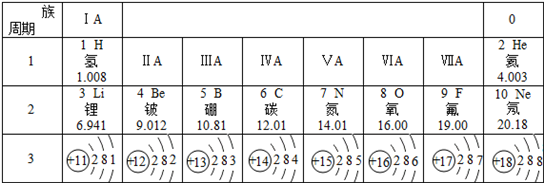
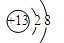 ;与该离子电子层结构相同的带一个单位负电荷的阴离子的符号是F-;
;与该离子电子层结构相同的带一个单位负电荷的阴离子的符号是F-;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com