
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
瘦肉精是一类对人体健康危害极大的化学物质,政府已严禁在猪饲料中添加瘦肉精。常见的瘦肉精化学式为C12H18OCl2N2,下列有关这种瘦肉精的说法中正确的是( )
A. 是一种无机化合物
B. 分子中碳、氢、氧三种元素的质量比为72:9:8
C. 相对分子质量为277g
D. 由C12H18O、Cl2、N2三种分子组成
B 【解析】 A、根据含有碳元素的化合物叫有机化合物,简称有机物.碳的氧化物、碳酸盐、碳酸虽含碳,但其性质与无机物类似,因此把它们看作无机物.可判断瘦肉精是一种有机物.故A错误; B、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;可得瘦肉精分子中碳、氢、氧三种元素的质量比为:(12×12):18:16=72:9:8;故B正确; C、根据相对分子的质量为组成分子的各...查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
人们常在可燃物建筑材料中添加阻燃剂以防止火灾。Mg(OH) 2是一种常见的阻燃剂,在380℃时分解成水蒸气和耐高温的MgO,并吸收大量的热。下列说法错误的是( )
A. Mg(OH)2分解吸热能降低可燃物的着火点
B. Mg(OH)2分解吸热能降低可燃物的温度
C. Mg(OH)2分解的产物能使可燃物与氧气隔绝
D. MgCO3比CaCO3易分解,也可作阻燃剂
A 【解析】本题考查的是灭火的原理和方法,灭火的原理:清除可燃物或使可燃物与其他物品隔离,隔绝氧气或空气,使温度降到可燃物的着火点以下。 A、着火点是物质的固有的属性,是不会改变的,只能改变可燃物的温度,故A错误; B、Mg(OH)2分解吸热能降低可燃物的温度到可燃物的着火点以下,故B正确; C、Mg(OH)2分解的产物水蒸气和耐高温的MgO,可以隔绝氧气或空气,故C正确;...查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
下图是甲、乙、丙三种物质的溶解度曲线,下列说法不正确的是

A. 甲的溶解度受温度影响最大
B. 10℃时,三种物质的溶解度大小顺序为丙>乙>甲
C. 30℃时,乙、丙两种物质的饱和溶液溶质质量分数相等
D. 50℃时,分别将40g甲、乙两种物质放入100g水中,均得到饱和溶液
D 【解析】A、根据图示的三种物质的溶解度曲线的线型,甲物质的溶解度曲线为“陡升型”,溶解度受温度影响较大;而乙、丙两物质的溶解度曲线呈“缓升型”,溶解度受温度影响较小;因此,三种物质中甲的溶解度受温度影响最大,故A正确;B、10℃时甲、乙、丙三种物质的溶解度曲线的位置关系为:丙物质的溶解度曲线在最上方而甲物质的溶解度曲线在最下方,因此,10℃时,三种物质的溶解度大小顺序为丙>乙>甲,故B正...查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
下列实验操作不符合规范的是( )
A. 点燃可燃性气体之前检验气体的纯度 B. 蒸发滤液时用玻璃棒不断搅拌滤液
C. 通过口尝来确定实验室中某种试剂的味道 D. 用酒精灯加热试管里的固体时先预热
C 【解析】 可燃性气体在点燃之前必须进行验纯,否则可能发生爆炸,A正确;蒸发滤液时用玻璃棒不断搅拌可以防止由于局部温度过高造成暴沸,B正确;实验室中很多药品都不能进行品尝,禁止口尝药品,防止中毒,所以C错误;加热固体必须先进行预热,再进行集中加热,D正确;所以答案选C。查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的的是( )
选 项 | 物质(杂质) | 操作方式 |
A | Cu(Fe) | 加足量稀硫酸,充分反应后过滤 |
B | CO(O2) | 缓慢通过灼热铜网 |
C | NaCl溶液(Na2CO3) | 加盐酸至恰好不再产生气泡为止 |
D | FeSO4溶液(CuSO4) | 加入足量铁屑,充分反应后过滤 |
查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
镍氢充电电池有着广泛应用,镍(Ni)及其化合物能发生下列反应:
①Ni+2HCl=NiCl2+H2↑ ②NiO+2HCl=NiCl2+H2O
③NiO2+4HCl=NiCl2+Cl2+2H2O
对上述反应的分析判断错误的是
A. 镍能与氧化铜溶液发生置换反应 B. NiCl2能与NaOH溶液发生复分解反应
C. 反应②和③都是复分解反应 D. 反应①、③中Ni的化合价都发生了变化
C 【解析】A、Ni能置换酸中的氢说明镍的金属性排在氢前所以一定能够置换出氯化铜中的铜;故对 B、氯化镍与氢氧化钠能发生复分解反应,因交换成分有沉淀氢氧化镍生成所以正确;故对 C、②符合③因反应后生成了三种物质不是复分解反应. D、①中有单质形式变成了化合物形式,化合价一定改变;③中根据化合物中元素化合价代数和为零,反应物中镍的化合价为+4价,生成物中镍的化合价为+2价,也...查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是( )


查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:填空题
(1)下图是一种家用电热水壶,所用材料属于合金的是________ (填字母序号,下同),属于单质的是_______, 属于合成材料的是____;

(2)学习化学需要在宏观物质的性质与其微观结构之间建立联系。
1个CO2分子由_____构成。在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是____,这三种物质的水溶液中pH<7的是______。
(3)A~G七种物质之间具有如下图所示转化关系。已知:A是一种含铁的矿石的主要成分,其中金属与非金属元素的原子个数比为1:2;B中铁的质量分数为70%;C是有刺激性气味的无色气体,它是形成酸雨的物质之一;F可溶于G的稀溶液并产生气体,该气体是有利于环境保护的理想燃料。请回答下列问题:
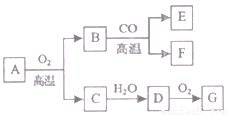
①A的化学式为______ ,已知A转化为B时金属元素的化合价升高,则A中非金属元素的化合价是____。
②B与CO反应的化学方程式是______________。
③C→D反应的化学方程式是________。
④B与G的稀溶液反应的化学方程式是________________。
A D BC 一个碳原子和两个氧原子 氢氧化钠、氯化钠 硫酸 FeS2 -1 Fe2O3+3CO2Fe+3CO2 SO2+H2O=H2SO3 Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 【解析】 (1)根据合金的概念,合金中必须有金属,不锈钢外壳是合金;单质是由一种元素组成的纯净物,纯铜导线属于单质;合成材料包括塑料、合成纤维、合成橡胶;聚氯乙烯线套和酚醛塑料手柄属于塑料...查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:实验题
(1)实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验。
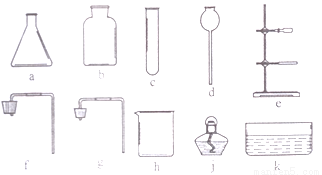
①要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是________(填序号),收集氧气应采取_______法。
②提纯粗盐时,过滤需要选用上述仪器中的________ (填序号), 除此之外还缺少的仪器是滤纸、____ 、_______ (填名称)。
(2)美羊羊同学在购买回的袋装薯片中发现还有一个小袋,上面标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色的,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3;灰白色粉末应该含有CaCO3和Fe;为验证自己的判断,美羊羊同学打算进行实验探究,请你一同参与。
(实验目的)证实灰白色粉末中含有CaCO3和Fe。
(实验设计)装置如下图所示:
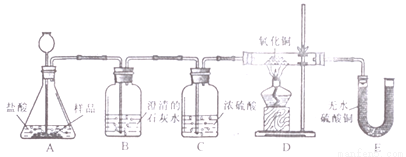
(实验预测与分析)
①若要证实样品中含有CaCO3,观察到的实验现象是____,B中发生反应的化学方程式为____________。
②若要证实样品中含有Fe, E中应观察到的现象是________。此时C装置的作用是______。
③看了美羊羊同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式_________。
adf 向上排气或排水法 eh 漏斗 玻璃棒 样品表面有气泡产生 Ca(OH)2+CO2=CaCO3↓+H2O 无水硫酸铜变成蓝色 干燥气体 Ca(OH)2 【解析】(1)①制取较多的O2,应用锥形瓶,制取过程中可以添加反应物,应用长颈漏斗,并用f封闭锥形瓶和导出气体;因氧气的密度大于空气的密度,并不易溶于水,所以可以用向上排空气法或排水法收集气体;②过滤要用到的仪器有:铁架台、烧杯、漏斗、...查看答案和解析>>
科目: 来源:四川省绵阳市2018年中考化学试卷 题型:单选题
我市有丰富的石灰石资源,为了测定某地石灰石中碳酸钙的质量分数,取7.5g样品放入烧杯,加入稀盐酸至恰好不再产生气体时消耗34.7g,放出的气体在常温下体积为1.1L。
(1)常温下CO2气体的密度为2.0g/L,则上述反应放出气体的质量为 g。
(2)如石灰石中的杂质均不溶于水且不与盐酸反应,计算石灰石中CaCO3的质量分数和反应所得溶液中溶质的质量分数(计算最终结果保留1位小数)。
C 【解析】 (1)二氧化碳的质量m=ρV=2.2g. (2)设碳酸钙的质量为x,生成的氯化钙的质量为y, 则CaCO3+2HCl═CaCl2+H2O+CO2↑, 100 73 111 44 x y 2.2g 100:x ="111:y" ="44:2.2g" , 解得x=5g,y=5.55g, 该样品中碳酸钙的质量分数为×100%=66.7%...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com