
科目: 来源:北京市2018年中考化学试卷 题型:单选题
电解水实验如下图。下列说法正确的是( )

A. 试管2中得到H2 B. 产生H2与O2的体积比约为1:2
C. 该实验说明水是由H2和O2组成 D. 可用带火星的木条检验生成的O2
D 【解析】 A、电解水实验中,与正极相连的试管中收集的是氧气,故A错误; B、电解水时,产生H2与O2的体积比约为2:1,故错误; C、水通电后生成氢气和氧气,氢气和氧气是由氢元素和氧元素组成,故该实验说明水是由H、O元素组成,水是纯净物,水中不含有氢气和氧气,故错误; D、氧气具有助燃性,可使带火星的木条复燃,故正确。故选D。查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:单选题
用下图装置进行实验。下列现象能证明空气中O2的含量的是( )
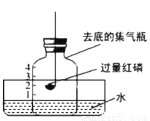
A. 红磷燃烧,产生白烟 B. 瓶中液面先下降,后上升
C. 瓶中液面最终上升至1处 D. 水槽中液面下降
C 【解析】 A、红磷燃烧,产生白烟,说明氧气支持燃烧,不能说明氧气的含量,故错误; B、瓶中液面先下降,后上升,说明反应放热,不能具体的说明氧气的含量,故错误; C、瓶中液面最终上升至1处,说明空气中氧气占总体积的1/5,正确; D、水槽中液面下降只能说明空气中氧气的体积减少,不能具体的说明氧气的含量,故错误。故选C。查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:单选题
已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g。

①~⑤所得溶液属于饱和溶液的是( )
A. ①③ B. ②④ C. ②⑤ D. ④⑤
C 【解析】 根据20℃时,NaCl和NaNO3的溶解度分别为36g和88g可知,②、⑤中含有未溶解的NaCl和NaNO3,即所得溶液为饱和溶液。故选 C查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:单选题
依据下列20℃时的实验和数据回答10~11题。
已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g。

下列关于①~⑤所得溶液的说法不正确的是( )
A. 溶质质量:①<② B. 溶液质量:②<④
C. 溶质质量分数:①=③ D. ⑤中溶质与溶剂的质量比为9:10
D 【解析】 A、根据20℃时,NaCl和NaNO3的溶解度分别为36g和88g判断溶质质量:①中30g<36g,故①所得的溶液是不饱和溶液,故溶液中的溶质的质量为30g,②中加入60g的氯化钠,最多只能溶解36g的氯化钠,故溶液中的溶质的质量为36g,故溶质的质量①<②,正确; B、②中最多溶解氯化钠的质量为36.0g,故所得溶液的质量为136g,④中60g的硝酸钠完全溶解,故...查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:单选题
氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如下。下列说法不正确的是( )

A. 甲中氮、氢原子个数比为1:3 B. 乙的相对分子质量为32
C. 两种生成物均为化合物 D. 生成的丙与丁的分子个数比为1:2
D 【解析】 根据微观示意图判断化学方程式为4NH3+5O2 4NO+ 6H2O。 A、甲物质是NH3,其中氮、氢原子个数比为1:3,故A正确; B、乙物质是O2,O2的相对分子质量为16×2=32,故B正确; C、由图可知,两种生成物是NO和H2O,都是由两种元素组成,故均为化合物,故正确; D、由方程式可知,生成的丙与丁的分子个数比为4:6=2:3,故错误。故选...查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:填空题
补齐连线。从13-A或13-B中任选一个作答,若均作答,按13-A计分。
查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:填空题
干热岩是地层深处的热岩体。下图为利用其发电的示意图。

(1)将干热岩的热量传递到热交换器的物质是______。
(2)从微粒的角度分析,水变为水蒸气时,变化的是_________。
水/水蒸气; 分子间间隔。 【解析】 (1)据图判断将干热岩的热量传递到热交换器的物质是水/水蒸气; (2)从微粒的角度分子,水变为水蒸气时,变化的是水分子的分子间间隔增大,而分子的种类没有发生变化;查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:简答题
H2O2可作增氧剂。常温下,用4%H2O2溶液进行实验,研究pH对H2O2分解所得溶液中氧量的影响,测定结果如图。

(1)H2O2分解的化学方程式为____________________。
(2)分析如图得到的结论是_______________。
2H2O2=2H2O+O2↑; 在常温下,当pH值在8-12之间时,随pH值增大,溶氧量先增大后减小,且在pH值在10-11中间时,溶氧量达到最大值。 【解析】 (1)H2O2分解生成氧气和水,反应化学方程式为2H2O2=2H2O+O2↑; (2)根据图中信息判断在常温下,当pH值在8-12之间时,随pH值增大,溶氧量先增大后减小,且在pH值在10-11中间时,溶氧量达到最大值。...查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:简答题
阅读下面科普短文。
化石能源是目前应用最广泛的能源,但其储量有限,不可再生。《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。

由上图可见,太阳能、风能等其他可再生能源在能源结构中所占比例日益增多。太阳能的利用是热门研究方向之一。例如,通过光催化可将H2O、CO2转化为H2、CO、CH4、CH3OH(甲醇)等太阳能燃料,示意图右图。

随着科技的进步,能源将得到更充分的利用。例如,利用照明灯、人体散发的热量灯生活中随处可见的废热发电。我国研发的“柔性、可裁剪碲化铋(Bi2Te3)/纤维素复合热点薄膜电池”,能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电。

在新能源的开发和利用中,化学起着不可替代的作用。
依据文章内容回答下列问题。
(1)比较2015、2030和2050年能源结构中的化石能源,所占比例降低的是_____________。
(2)H2O、CO2转化得到的太阳能燃料中,属于氧化物的是_____________;该过程属于_______________(填“物理”或“化学”)变化。
(3)复合热点薄膜电池中Bi2Te3由_______种元素组成。
(4)下列说法正确的是 ____________(填序号)。
A.能源结构向多元、清洁、低碳转型 B.科技进步会促进能源的利用
C.石油和太阳能属于可再生能源 D.生活中的废热可转化为电能

查看答案和解析>>
科目: 来源:北京市2018年中考化学试卷 题型:流程题
炼铁的主要原料是赤铁矿(主要成分是Fe2O3)、焦炭、空气等,转化过程如下:

(1)②中,反应为CO2+C 高温2CO,其中化合价发生改变的元素是______。
(2)③中,CO与Fe2O3反应的化学方程式为_____________________。
C或碳元素; Fe2O3+3CO 2Fe+3CO2。 【解析】 (1)CO2中C的化合价为+4,氧元素的化合价为-2,C单质的化合价为0,CO中C的化合价为+2,氧元素的化合价为-2,即该反应中碳元素化合价发生改变; (2)一氧化碳与氧化铁在高温的条件小反应生成铁和二氧化碳,反应方程式为:Fe2O3+3CO 2Fe+3CO2查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com