
科目: 来源: 题型:
【题目】如下图中A、B分别表示某微粒的结构示意图,回答下列问题。

(1)若A表示某稀有气体元素的原子,则该元素的单质的化学式为_________________。
(2)若B表示某元素的原子,则Y=____________,该元素的原子在化学反应中容易____________(填“失去”或“得到”)电子。
(3)若A是阳离子的结构示意图,则X可能是下列中的________________(填字母序号)
A.8 B.10 C.11 D.12
(4)若A中X=13,则A、B所表示的元素形成的化合物的化学式为_______,该物质是由__________构成。
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。

(1)甲同学:点燃红磷立即伸入瓶中并塞上瓶塞。待红磷燃烧停止并冷却后,打开止水夹,观察到集气瓶中吸入水的体积约占集气瓶容积的________________。
(2)乙同学:用碳替代红磷,完成上述试验,发现集气瓶内并没有吸入水,其原因是_________________
(3)丙同学:向集气瓶中加入少量的________溶液,然后完成乙同学的实验,得到了与甲同学相同的实验结果。
(4)试写出加入物质发生反应的化学方程式________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】侯德榜是我国化学工业的奠基人,纯碱工业的创始人。他发明的“侯氏制碱法”,缩短了生产流程,减少了对环境的污染,在人类化学工业史上写下了光辉的一页。侯氏制碱法的主要反应为:
NH3 + CO2 + H2O + NaCl = NaHCO3 + NH4Cl ,

他利用生成物中的NaHCO3溶解度较小,一经生成便会大量析出,能够很容易的分离出NaHCO3。
化学小组同学模拟“侯氏制碱法”完成以下实验:10℃时,向92.6g饱和NaCl溶液中先通入足量NH3共3.4g,再通入一定量CO2至恰好完全反应。请计算:(不考虑溶解在溶液中的NH3和CO2的质量)。
(1) NH4Cl可作为氮肥使用,其中氮元素的质量分数(只写出计算过程)___________。
(2) 以上反应中消耗CO2的质量是多少?
(3) 反应后称量溶液中析出NaHCO3晶体的质量为14.4g,则剩余溶液的质量是多少?
查看答案和解析>>
科目: 来源: 题型:
【题目】春节期间燃放烟花爆竹会使空气中有害气体SO2的含量增加,为粗略测定空气中SO2的含量,化学小组的同学们设计了如下图所示的实验装置进行实验:

【资料】
①SO2+I2+2H20=H2SO4+2HI,碘遇淀粉能使淀粉显蓝色,而HI溶液不能使淀粉显蓝色。
②我国空气质量标准中SO2浓度限值(mg/m3)如下表;
一级标准 ≤0.15
二级标准 ≤0.50
三级标准 ≤0.70
【实验步骤】
①检查气密性;
②向C装置中加入1.0mL溶质质量分数为1.27×10﹣6 g/mL的碘水(ρ≈1.0g/mL),滴入2~3滴淀粉溶液,此时溶液显蓝色;
③打开弹簧夹___________(填“a”或“b”),关闭另一个弹簧夹,抽拉注射器吸取250mL空气,再开、闭相应弹簧夹,缓缓推气体进入C装置,重复上述操作多次。当C中溶液颜色____________时,停止推动注射器的活塞;
④实验数据处理。
请回答下列问题:
(1)完善步骤③的内容________________;_____________。
(2)检查此装置气密性的操作是:_______________;
(3)该小组在同一地点进行了3组实验,推动活塞次数记录如下表(每次抽气为250mL)。进行3组实验的目的是_____________;综合3次实验数据分析:该测定地点的空气质量属于_________级标准
实验序号 | 推动次数 |
1 | 3 |
2 | 5 |
3 | 4 |
查看答案和解析>>
科目: 来源: 题型:
【题目】小新在实验室制取二氧化碳时发现:如果用大理石和稀硫酸混合制二氧化碳,一开始产生一些气泡,可是很快气泡产生的速度越来越慢,最终停止了。其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。因此通常不选用大理石与稀硫酸反应制取二氧化碳。对此,小新产生了疑问并大胆猜想展开实验。

(1)【猜想一】选择合适的硫酸的浓度能使反应快速进行
【进行实验】在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,实验选取5种浓度(如右图)的硫酸分5组完成,每次记录15分钟内生成气体的体积,记录在下表:
试管编号 | 气体体积(mL) |
1 | 35 |
2 | 47 |
3 | 55 |
4 | 51 |
5 | 42 |
(2)【猜想二】选择合适的温度可以使反应快速进行
【进行实验】向5只分别盛有1g、直径为2mm大理石的大试管中各加入5mL相同浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
试管编号 | 温度℃ | 现象 |
A | 40 | 有气泡 |
B | 50 | 气泡比A试管多 |
C | 60 | 气泡明显比B号试管多,持续时间更长 |
D | 70 | 大量气泡产生,与常温用盐酸反应相似 |
E | 80 | 反应非常剧烈,大理石迅速溶解并产生大量气体 |
(3)【实验分析】
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适的是___________%。
②在合适的硫酸浓度下,应选择最合适的反应温度为___________℃。
③除选用合适温度和浓度硫酸之外,在反应过程中,为防止微溶物硫酸钙覆盖在大理石上,应增加_________操作,更有利气体的制备。
(4)你认为还可以研究___________对该反应速率的影响,请你设计实验简述实验步骤______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列与水有关的问题:

(1)右图是电解水装置,收集到氢气的是试管____________,该反应的化学方程式为______________。
(2)海水淡化可以解决淡水不足的问题,右图是一个简易的海水淡化装置,阳光照射一段时间后b处海水的溶质质量分数会变______________(填“大”或“小”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是自来水厂净水过程示意图,试回答下列问题:
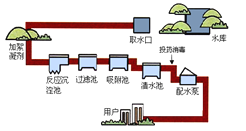
(1)自来水厂生产自来水时使用的净水方法有___________(填写字母序号)。
A.沉淀 B.过滤 C.消毒 D.吸附
(2)吸附池通常添加的吸附剂是______________。
(3)过滤池主要是要除去_____________杂质(填写字母序号)。
A可溶性的 B.难溶性的 C.有色有味的 D.沸点高的
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是小文在家里找到的一些物品。

(1)下列VC泡腾片的主要成分中属于有机物的是__________(填字母序号)。
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
(2)在一个试管中加入少许MnO2,再倒入彩漂剂,会产生大量气泡,此气体是______________。
(3)洁厕灵在使用时要避免和大理石地面接触,其原因是____________(写出化学反应方程式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】尿素[CO(NH2) 2]是蛋白质代谢的产物。下列关于尿素的说法中不正确的是
A.尿素是一种氮肥
B.尿素由1个碳原子、1个氧原子、2个氮原子和4个氢原子构成
C.尿素中碳、氧两种元素的质量比为3︰4
D.尿素中氮元素的质量分数为46.7%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com