
科目: 来源: 题型:
【题目】某同学用过氧化氢溶液和二氧化锰制取氧气,化学方程式为:2H2O2
2H2O +O2↑,该同学将50g过氧化氢溶液和1 g 二氧化锰混合,完全反应后,称量剩余的混合物质量为49.4g。
求:(1)反应产生氧气的质量是 g。
(2)该同学所用过氧化氢溶液的溶质质量分数是多少(列式计算)?
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是一门以实验为基础的科学。请根据下列仪器和实验装置回答有关问题:

(1)仪器②的名称是
(2)用①②③组合可制备CO2,写出实验室用此装置制备CO2的化学方程式 。
(3)收集CO2应选用装置 (填“④”或“⑤”)
(4)利用图⑥所示装置(集气瓶中预先装满CO2气体)来验证CO2的性质,先加入足量氢氧化钠溶液,观察到的现象是气球 (填“变大”、“变小”或“不变”),反应方程式为_______;再加入足量的盐酸,观察到的现象是气球 (填“变大”、“变小”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)用化学符号填空
①2个氢原子______;②2个水分子______;③能形成硫酸型酸雨的空气污染物是 。
(2)右图甲、乙表示的是同一种元素Al,据图回答
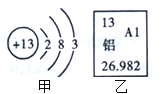
④原子的核电荷数是 ;
⑤在化学反应中,原子易失去电子形成 。
(3)下图是某化学变化的微观示意图,其中“○”和“●”分别代表不同元素的原子,据图回答问题:
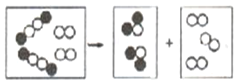
⑥该反应、生成物的分子个数比为 ;
⑦该反应的基本类型为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】分析处理图表中的信息是学习化学的一种重要方法。
(1)下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 |
①40℃时,氯化钠的溶解度为_____g。
②碳酸钠的溶解度随温度的升高而________(填“增大”或“减小”)。在20℃时,将100g的水加入30 g碳酸钠中,充分搅拌后得到的是________(填“饱和溶液”或“不饱和溶液”)。
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是______。
(2)将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式_______。右图是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是_______(填标号)。

查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜是Zn以主要添加元素的铜合金。黄铜渣中约含Zn-7%、ZnO-31%、Cu-50%、CuO-5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):

已知:ZnO+H2SO4=ZnSO4+H2O; CuO+H2SO4=CuSO4+H2O
(1)步骤Ⅰ中产生气体的化学方程式为 。
(2)溶液A中的金属阳离子有 (填化学式)
(3)步骤Ⅰ、Ⅱ中均包含的操作名称为 ,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是 。
(4)溶液A (填“大于”、“小于”或“等于”)溶液C的质量。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组在研究由Fe2+制备Fe(OH)2:
(1)【查阅资料】甲同学查阅资料后,得到Fe(OH)2如下信息:

(2)【实验设计】甲同学查阅资料后设计如下实验方案:按照下图进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行.

最终在 容器中观察到白色沉淀,该实验中涉及到主要现象的化学方程式有(可以分步书写): , .反应开始打开C的目的是 .
(3)【意外发现】实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?甲对上述实验中出现灰绿色或绿色的现象的解释是: .
(4)【阐释异议】乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2·nH2O所致.用热水浴的方式加热生成的绿色沉淀,观察到沉淀由绿变白的趋势.写出该实验中支持乙同学观点的化学方程式 .
(5)【深入验证】欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路. .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某种治疗胃病药品的主要成份是铝碳酸镁片,化学式为AlaMgb(OH)16CO3·4H2O,假设药品中的其它成份受热不分解、不溶于水且不与稀硫酸反应.某研究性学习小组设计了如下实验探究铝碳酸镁片的组成.

【实验一】取m g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16g,装置D增重0.44g.
(1)铝碳酸镁片加热分解的产物为Al2O3、MgO、CO2和水,则为分别测定CO2和水的质量,装置C和D中盛放的药品应选择:C , D (填序号).
①浓硫酸 ②碱石灰 ③氯化钙 ④纯碱
(2)实验开始前先通入一定量空气,其操作方法是关闭弹簧夹 ,打开弹簧夹 ,目的是 .
(3)一段时间后,打开弹簧夹 ,关闭弹簧夹 ,点燃酒精灯加热,充分反应后,停止加热,继续通入空气至玻璃管冷却的目的是 (填序号).
①排净空气防爆炸
②防止空气中水和二氧化碳进入C、D影响测定
③使生成水和二氧化碳进入C、D被充分吸收
【实验二】另取m g该药片,加入100 g 9.8%的稀硫酸,充分反应后滤去不溶物,得到含有MgSO4和Al2(SO4)3等溶质的滤液,向滤液中逐渐加入足量的稀NaOH溶液,产生沉淀的物质的质量与加入NaOH质量的关系如图.
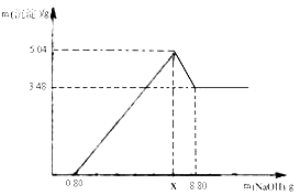
已知:MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,
Al2(SO4)3+6NaOH=2Al(OH)3↓+3Na2SO4,
Al(OH)3+NaOH=NaAlO2+2H2O,
Mg(OH)2不溶于NaOH,NaAlO2可溶于水.
(1)图中NaOH加入0.80g,仍没有沉淀,说明滤液中含 .当加入NaOH的质量到x时,生成的沉淀有 ,其中Al(OH)3的质量是 g,则x= g.
(2)有医生建议患有严重胃溃疡的患者最好慎用该药,试用你所学的知识解释这样建议的理由是 .
(3)试确定铝碳酸镁的化学式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合图示实验装置,回答下列问题:
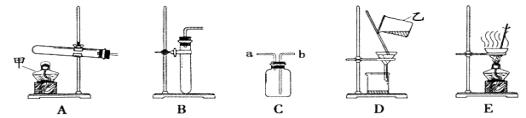
(1)写出图中仪器甲、乙的名称:甲 ,乙 .
(2)实验室用高锰酸钾制取氧气,发生装置可选择图中的 (填标号),写出该反应的化学方程式 .用充满水的装置C收集氧气,则氧气需从 (填“a”或“b”)端通入.
(3)实验室制取二氧化碳的化学方程式是 ,用装置C收集二氧化碳,验满时,燃着木条应放在 (填“a”或“b”)端.
(4)用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练.
①对固液残留物进行过滤,应选择图中装置 (填标号),过滤时玻璃棒的作用是 .
②取上述少量滤液进行蒸发,析出的固体中一定含有的物质是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com