
科目: 来源: 题型:
【题目】对于下图的说法中,错误的是
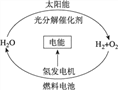
A. 燃料电池能够使化学反应产生的能量转化为电能
B. 该氢能源的循环体系能够实现太阳能转化为电能
C. 在此循环中发生了反应:2H2O通电 2H2↑+O2↑
D. 目前化学家急需解决的问题是寻找更加合适的催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】作业检查了,妈妈精心为小云准备了如下的食谱:主食:馒头,米饭;配菜:红烧肉、豆腐汤、牛肉干。你认为食谱中还应添加( )
A. 炒鸡蛋 B. 黄瓜 C. 牛奶 D. 红烧鱼
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验,不能成功的是
A.收集一瓶氧气,观察颜色 B.观察颜色来区分高锰酸钾和氯酸钾
C.闻气味来区分白酒和白醋 D.用10毫升量筒量取5.56mL的水
查看答案和解析>>
科目: 来源: 题型:
【题目】10℃时,向两只试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图1所示的现象。图2是甲、乙两种物质的溶解度曲线。下列说法错误的是
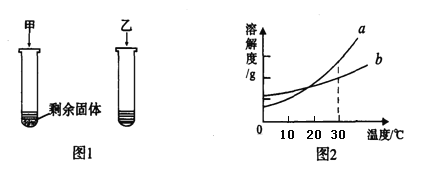
A. 10℃时,甲一定是饱和溶液
B. 10℃时,乙一定是不饱和溶液
C. 给两支试管加热至30℃,甲、乙溶液的溶质质量分数相等
D. 30℃时,将两支试管溶液制成饱和溶液,则它们的质量:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】学做实验时记录了下列实验现象,其中正确的是( )
A. 红磷在空气中燃烧,产生大量白雾
B. 细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成
C. 少量高锰酸钾固体溶于水,得到浅绿色溶液
D. 分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象能正确反映其对应实验操作的是
|
|
|
|
A.加热一定质量的高锰酸钾 | B.用等质量、等质量分数的双氧水制取氧气 | C.向一定质量的大理石(杂质不参加反应)中滴加稀盐酸 | D.某温度,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】水和溶液在生产、生活中起着十分重要的作用。
(1)走近臭水沟就闻到臭味,请用微粒的观点解释______________________ 。为了除去水的臭味和颜色,可以用______________ 进行吸附。
(2)检验水是硬水还是软水可用的物质是____________ 。硬水中含有较多____________(填离子符号),生活中将硬水软化常用的方法是____________ 。使用久的水壶内壁会形成水垢,可用厨房中的____________ 浸泡除去。
(3)我们常在水中加洗洁精清洗餐具上的油污,这是因为洗洁精具有___________作用。
(4)水可以用于灭火,其原理是_____________________________。
(5)电解水时电源负极产生的气体是___________(填化学式),正极和负极产生气体的体积比为___________,其反应的化学方程式_______________。
(6)冬季常在积雪上撒盐,目的是________________。
(7)高温下,铁能和水蒸气反应生成四氧化三铁和一种可燃的气体单质,该反应的化学方程式为____________。
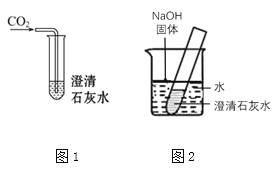
(8)下图1是将CO2通入澄清石灰水,图2中往烧杯里加入氢氧化钠固体,两只试管中澄清石灰水都变浑浊。图1中石灰水变浑浊的化学方程式是__________ ,图2中石灰水变浑浊的原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】日常使用的干电池是一种锌锰电池,它的构造是:负极为锌做的圆筒,正极是一根碳棒,它的周围被二氧化锰,碳粉和氯化铵的混合剂所包围,总称为"碳包"。碳包和锌筒之间填充着氯化铵、氯化锌的水溶液和淀粉等组成的糊状物。废旧干电池随意丢弃会造成环境污染。学校兴趣小组同学准备对废旧的干电池进行探究。
(一)拆解干电池,得到铜帽、锌皮、碳棒、黑色粉末等物质。
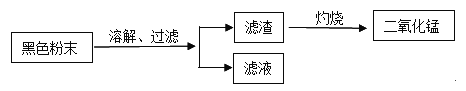
(二)回收二氧化锰并测定碳粉与二氧化锰的质量比:
(1)干电池使用时将化学能转化成___________能。
(2)上述操作中灼烧的目的是___________;
(3)同学们将过滤后得到的滤渣干燥后称得质量为25克,充分灼烧后冷却称得剩余固体质量为20克,则滤渣中二氧化锰与碳粉的质量比为___________。经分析,此结果偏大,老师指出同学们在实验中缺少一步操作,该操作是___________。
(4)为验证二氧化锰,同学们用A、B两支洁净试管,分别取5毫升3%的过氧化氢溶液,往A试管中加入少量上述实验灼烧后得到的固体,如果出现___________的现象,说明为二氧化锰。反应的化学方程式为___________。
(三)用拆解得到的锌皮(含杂质)制取硫酸锌晶体。
实验步骤:①将剪碎后的锌皮放入烧杯中,加入足量的稀硫酸,充分反应;②将上述反应后的混合物过滤。③将滤液加热浓缩、_____、过滤,得到ZnSO4·7H2O晶体。
(5)步骤①中反应方程式为___________,将锌皮剪碎的目的是__________。
(6)步骤②需要的仪器有铁架台、烧杯、___________和玻璃棒,玻璃棒的作用是___________。
(7)步骤③缺少的操作是____________。
(四)测定锌皮中锌的质量分数。同学们设计了如下实验装置,取1克锌皮放于试管中,实验中将注射器内50毫升稀硫酸(足量)完全注入试管中。当试管中不再产生气泡时立刻读数得到量筒中水的体积为350毫升。已知实验条件下氢气的密度为0.09g/L。
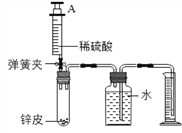
(8)计算该锌皮中锌的质量分数___________。(写出计算过程,结果保留两位小数)
(9)上述方法测得的锌的质量分数偏大,不可能的原因是____________
A.没等装置冷却就读数
B.锌皮中含有少量铁
C.试管中有气体没有排出
D. 将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com