
科目: 来源: 题型:
【题目】根据下列装置图,回答有关问题:

(1)写出装置图中标号仪器的名称:①__________,②__________。
(2)实验室选用装置A作为氧气的发生装置,化学方程式为______________________;选用锌粒与稀硫酸反应制取氢气,化学方程式为______________________;氧气和氢气均可选用装置__________(填字母)作为收集装置。
(3)实验室选用大理石与稀盐酸反应制取二氧化碳,利用如图所示装置,可以得到纯净、干燥的二氧化碳。用化学方程式表示饱和碳酸氢钠溶液的作用:______________________;装置接口的连接顺序:发生装置→______,______→______,______→收集装置(填数字)。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.氧气的化学性质比较活泼,属于可燃物
B.氮气的化学性质不活泼,可用于食品防腐
C.空气质量报告中所列的空气质量级别越大,空气质量越好
D.二氧化碳属于空气污染物
查看答案和解析>>
科目: 来源: 题型:
【题目】葡萄糖(C6H12O6)是一种重要营养物质,下列关于葡萄糖的说法中,正确的是( )
A. 葡萄糖由6种碳元素、12种氢元素和6种氧元素组成
B. 葡萄糖由6个碳原子、12个氢原子和6个氧原子构成
C. 每个葡萄糖分子中所含原子个数为24
D. 每个葡萄糖分子中碳、氢、氧元素质量比为1:2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是一门以实验为基础的科学。
(1)控制变量是实验探究的重要方法,完成下表:
实验 | 探究人体吸入的空气与呼出的气体有什么不同 | 探究分子的运动 | 探究铁制品锈蚀的条件 |
设计 |
|
|
|
分析 | 本实验需要控制: ①集气瓶规格相同; ②________相同。 | 本实验说明: ①分子在不断运动; ②影响分子运动速率的因素有__________。 | 本实验说明: 铁制品锈蚀的条件之一是与__________接触。 |
(2)某化学学习小组在实验室练习配制一定溶质质量分数的溶液。
①配制50g质量分数为6%的氯化钠溶液,需要氯化钠的质量为__________g;用托盘天平称量所需的氯化钠时,若指针偏向左盘,应__________(填字母)至天平平衡。
A.增加氯化钠 B.减少氯化钠 C.向左移动游码 D.向右移动游码
②把50g质量分数为6%的氯化钠溶液稀释成质量分数为4%的氯化钠溶液,需要水的体积为__________mL(水的密度可近似看作1g/cm3);用量筒量取所需的水时,若俯视读数,得到的氯化钠溶液的质量分数__________(填“大于”、“小于”或“等于”)4% 。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与人类的生产、生活密切相关。
(1)化学与健康。
①钙能强壮骨骼,在人体中属于__________(填“常量元素”或“微量元素”)。
②在人体组织里,葡萄糖(C6H12O6)在酶的催化作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,该反应的化学方程式为______________________。
(2)化学与资源。
①在空气的成分中,稀有气体所占比率虽然很小,但有广泛的用途。写出氦气的化学式,并标出氦元素的化合价:__________。
②如图所示的简易净水器中,活性炭的作用是过滤和__________;打开汽水瓶盖时,汽水会自动喷出来,是因为压强减小,气体的溶解度__________(填“增大”或“减小”)。

(3)化学与能源。
①可燃冰主要含有甲烷水合物,如果在开采中甲烷气体大量泄漏于大气中,将比二氧化碳造成的__________效应更加严重。
②4.6g某化合物在空气中完全燃烧生成8.8g二氧化碳和5.4g水,写出该化合物中各元素的质量比:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】图中A~J是初中化学常见的物质,且分别是由H、O、S、Cl、Ca、Fe、Cu中的一种或几种元素组成的。A是理想的清洁、高能燃料,G的溶液呈蓝色;B、D、H、I是由两种元素组成的化合物,且I是红棕色固体;每个正方形包含的四种物质均为不同类别的物质。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
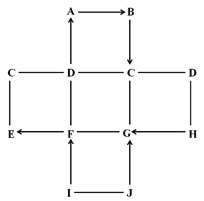
(1)写出化学式:A__________。
(2)写出化学方程式:
B转化为C的反应______________________,
H转化为G的反应______________________,
I转化为F的置换反应______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
【资料卡片】
(1)碳酸钠俗称纯碱、____。以纯碱和熟石灰为原料可以制烧碱,化学方程式为________。
(2)1921年,_______(填字母)发明了将制碱与制氨结合起来的联合制碱法,大大提高了原料的利用率。
A.拉瓦锡 B.道尔顿 C.侯德榜 D.张青莲
【定性实验】食盐是联合制碱法的主要原料之一,因此制得的纯碱中含有少量氯化钠。为了检验纯碱样品中存在氯离子,需要用到的药品是__________(填字母)。
A.氯化钡溶液 B.硝酸银溶液 C.稀硝酸 D.稀盐酸
【定量实验】将12.0g纯碱样品溶于水,加入足量氯化钡溶液,充分反应后,过滤、洗涤、低温干燥,得到19.7g沉淀。计算纯碱样品中碳酸钠的质量分数。__________(写出计算过程,结果保留一位小数)
【实验设计与评价】甲同学设计了如图实验装置,通过测量一定质量的纯碱样品与足量稀硫酸反应后产生二氧化碳的体积,进一步计算纯碱样品中碳酸钠的质量分数。

(1)检查装置的气密性时,起始状态量气管和水准管中液面相平,提高量气管,__________,证明该装置的气密性良好。
(2)乙同学认为该装置测得的二氧化碳的体积会偏小(不考虑操作上的失误),他的理由是______________________。
(3)丙同学认为该装置测得的二氧化碳的体积会偏大(不考虑操作上的失误),他的理由是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以白云石(主要成分为CaCO3·MgCO3)为原料制备氢氧化镁的流程如下图:
已知:①MgCO3![]() MgO+CO2↑,CaCO3
MgO+CO2↑,CaCO3 ![]() CaO+CO2↑ ;
CaO+CO2↑ ;
②反应器中发生的反应是 (NH4)2SO4 + MgO ![]() MgSO4 + 2NH3↑+ H2O 。
MgSO4 + 2NH3↑+ H2O 。
(1)实验室进行过滤操作时,玻璃棒的作用是__________________。
(2)该流程中,研磨的目的是__________________;轻烧的温度不超过________℃,经轻烧得到的固体的主要成分是__________________(写化学式)。
(3)该流程中,不考虑H2O,可循环利用的物质是__________________(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com