
科目: 来源: 题型:
【题目】下列有关空气的说法错误的是( )
A. 按质量计算,空气中含有氮气约78%,氧气约21%
B. 空气中各种成分的含量是相对稳定的
C. 空气是一种十分重要的天然资源
D. PM2.5是造成空气污染的主要污染物之一
查看答案和解析>>
科目: 来源: 题型:
【题目】下列日常生活中的做法可行的是( )
①大豆、花生和谷物被霉菌污染后,人不可食用,但可喂养家禽
②由于淀粉有遇碘变蓝的特性,可利用淀粉检验加碘食盐的真假
③喝牛奶、豆浆等富含蛋白质的食品可有效缓解重金属盐中毒现象
④低血糖病症发作时,吃馒头要比喝葡萄糖水见效快
⑤患有夜盲症的病人,多食用动物肝脏有利于保护视力
A.①③④ B.②④
C.②③⑤ D.③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】物质X的化学式为H2C2O4 , 可发生如下反应: aH2C2O4 ![]() bH2O↑+cCO2↑+dY↑
bH2O↑+cCO2↑+dY↑
取90g X,在t℃完全分解,产物通过足量浓硫酸,浓硫酸增重18g,另取90gX,在t℃完全分解,产物通过足量碱石灰(CaO和NaOH的固体混合物),碱石灰增重62g,则下列说法不正确的是(已知气体Y不与浓硫酸或碱石灰发生反应)( )
A.CO2的质量为44g
B.气体Y的质量为28g
C.气体Y可能为甲烷
D.方程式中b和c的比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】NH4Cl和NaCl的溶解度随温度变化如图所示,下列说法正确的是( ) 
A.NH4Cl的溶解度一定大于NaCl
B.将NaCl溶液降温一定会有NaCl固体析出
C.50℃时饱和溶液的溶质质量分数为50%
D.将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等
查看答案和解析>>
科目: 来源: 题型:
【题目】通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.
(1)现有H、C、N、O、Ca五种元素,请选用其中的元素写出下列物质的化学式: ①最简单的有机物;②空气中含量最多的气体;
③可做制冷剂的干冰;④常用作改良酸性土壤的碱 .
(2)澳大利亚工程师研制出新型太阳能电池的路灯将极大提高能量转化效率. ①如图所示物质中属于有机合成材料的是 .
②铝具有很好的抗腐蚀性能,原因是 .
(用化学方程式表示);灯材料使用的铝合金属于(填“纯净物”或“混合物”).
③太阳能电池板的主要材料是硅,硅的原子结构示意图 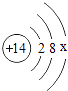 ,其中x= .
,其中x= . 
查看答案和解析>>
科目: 来源: 题型:
【题目】小刚在量取液体时,开始采用俯视读数为15mL,倒出一定量液体后又仰视读数为5 mL,则该同学倒出的液体的体积为( )
A.>10 mL B.<10 mL C.=10mL D.无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】高氯酸钠晶体(NaClO4H2O)可用于制备高氯酸.粗盐除去泥沙等不容性杂质后得到“精盐”(只含MgCl2、CaCl2两种杂质),以“精盐”为原料制备高氯酸钠晶体的流程如下:
【资料】高氯酸钠在较高温度下容易分解.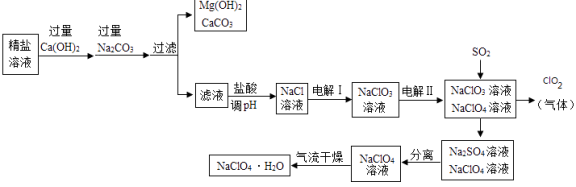
请回答下列问题:
(1)滤液中溶质除NaCl外还含有 .
(2)ClO2中氧元素的化合物是 .
(3)通入SO2是为了除去NaClO4溶液中少量的NaClO3 , 该反应的化学方程式为 .
(4)“气流干燥”时温度应控制在75°C~95°C之间,其原因是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】绿矾(FeSO47H2O)是硫酸法生产太白粉的主要副产物,可用于制备Fe2O3 , 复印用Fe3O4粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作.某研究性小组展开了系列研究. Ⅰ制备Fe2O3
【资料一】
①无水硫酸铜遇水变成蓝色的硫酸铜晶体.
②绿矾(FeSO47H2O)高温分解产生一种金属氧化物和几种气态非金属氧化物.
③SO2是无色有窒息性臭味的有毒气体,能使品红溶液褪色.
甲同学用如下装置制备Fe2O3并验证绿矾受热分解的其他产物;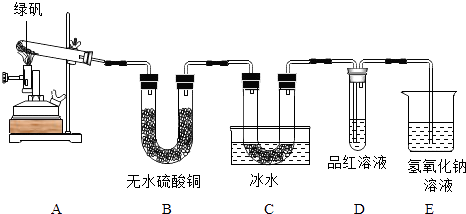
(1)实验过程中发现:A中有色固体生成,B中无水硫酸铜变蓝,C中U形管内有无色晶体(SO3)析出,D中品红溶液褪色,装置E的作用是 , 绿矾高温分解的化学方程式为 .
(2)Ⅱ制备Fe3O4 乙同学模拟生产复印用Fe3O4粉的实验流程如下:
【资料二】Fe(OH)2是一种白色难溶于水的固体,在空气中易被氧化.
FeSO4溶液中加入NaOH溶液,反应的化学方程式依次为① , ②4Fe(OH)2+O2+2H2O═4Fe(OH)3 . 由沉淀a获得Fe3O4的化学方程式为:Fe(OH)2+2Fe(OH)3═Fe3O4+4H2O
若制取Fe(OH)2 , 采取的实验操作是:向盛有5mL新制FeSO4溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶O2),胶头滴管的争取使用方法是(填字母).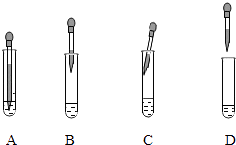
(3)Ⅲ制备还原铁粉 制备还原铁粉的工业流程如下: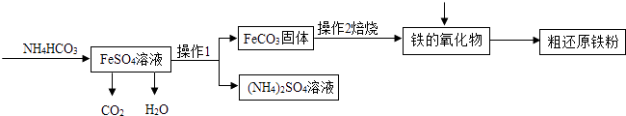
①操作1的名称是 , NH4HCO3和FeSO4溶液反应的化学方程式为 .
②若将14.06g粗还原铁粉(假设粗还原铁粉中杂质仅含少量FexC)在氧气流中完全反应,得到0.22g
CO2 , 将相同质量的粗还原铁粉与足量稀硫酸反应,得到0.48gH2(FexC与稀硫酸反应不产生H2).试通过计算确定FexC的化学式(请写出计算过程) .
③粗还原铁粉经加工处理后变成纯还原铁粉,纯还原铁粉和水蒸气在高温条件下也可制得四氧化三铁,同时生成一种气体.其装置如图所示: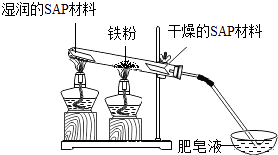
SAP材料吸水性强,湿润的SAP材料能为该反应持续提供水蒸气.实验开始一段时间后,观察到在肥皂液中有大量的气泡产生,此气泡用火柴即能点燃,同时有肥皂泡飘到空中.生成的气体是 , 干燥的SAP材料作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com