
科目: 来源: 题型:
【题目】小杰同学从家里带来一个小纸袋,上面写着“石灰干燥剂”,纸袋上信息如图,实验小组同学对该干燥剂进行如下探究。

【辨析推断】
(1)“石灰干燥剂”中的石灰是指__________(填字母)。
A.消石灰 B.生石灰 C.石灰石
(2)不可食用,幼儿勿取的原因__________。
【提出问题】该袋干燥剂的现有成份是什么呢?
【实验探究】分别取该石灰干燥剂进行如表实验,并记录。
实验目的 | 实验步骤 | 实验现象 | 实验结论 |
实验一:验证有无 CaCO3 |
| __________ | 样品中有碳酸钙 |
实验二:__________ |
| 无放热现象 | __________ |
【问题分析】同学们由上表现象结合已学知识综合分析后,认为该袋干燥剂的成份可能为:
①碳酸钙 ②碳酸钙和__________
【成分探究】取少量样品加水溶解,静置后取少量上层清液于试管中,再向试管中__________,观察到__________,证明该固体成分是两种物质。
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据下图所示的实验装置图填空。
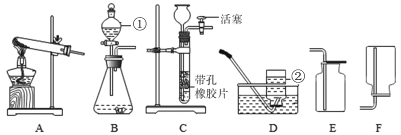
(1)D图中②的仪器名称为__________。
(2)实验室用B装置制取氧气时,发生反应的化学方程式为__________,
仪器①的作用是__________(写一点即可)。
(3)现有大理石、碳酸钠粉末、稀盐酸、稀硫酸,选择合适的物质用C装置制取CO2气体,其化学方程式为__________,在反应过程中,使反应停止的操作是__________。
(4)实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体。甲烷是一种无色无味、密度比空气小、极难溶于水的气体,则制取并收集甲烷的装置组合是__________,若用右图装置收集甲烷,气体应从_________端导入(选填“a”或“b”)。

(5)小明同学用锌粒和稀盐酸制取氢气,小华认为小明制取的氢气不纯,杂质气体除了水蒸气外还含有__________(填化学式),基于以上问题,两位同学最终设计了如下方案制取纯净、干燥的氢气,请回答下列问题。
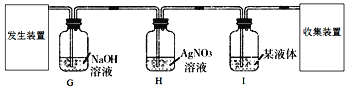
①H中硝酸银溶液的作用是__________;
②I中液体是__________(填名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A~G为初中化学常见物质,相互关系如图所示,“→”表示转化关系,“—”表示相互之间能发生反应(部分反应物、生成物及反应条件省略)。其中A、F是两种常见的氧化物;B、D是两种常见的碱; G可用作建筑材料;C常用于洗涤剂的生产;A、B、C、E所属物质类别不同。请回答下列问题。
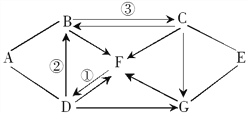
(1)A的化学式___________,G的化学式__________。
(2)D的用途有__________(写出一种即可)。
(3)写出化学反应①②③的化学方程式:
①__________;
②__________;该反应属于四种基本反应类型中的__________反应。
③__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学探究的重要途径是化学实验。请根据下列图示回答相关问题:
(1)某同学在配制100 g溶质质量分数为8%的氯化钠溶液前绘制了如下操作示意图,你认为该实验的正确操作顺序为____________(填字母序号)。
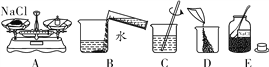
(2)经检测,该同学所配溶液的溶质质量分数偏大,其原因可能是________(填序号)。
①称量时,药品端忘垫质量相同的纸片 ②氯化钠固体不纯 ③量取水时,俯视读数 ④装瓶时,有少量溶液洒出
(3)我们在实验室内无论是用一定量固体配制溶液还是稀释溶液,最后都需要把配制的溶液装在试剂瓶中,盖好瓶塞并贴上标签,放到试剂柜中。通常标签中应包括__________和___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】20 ℃时,取18 g KNO3和18 g NaCl分别放入两只烧杯中,各加入50 mL水(水的密度为1 g/mL),充分溶解,现象如图甲所示;升温到50 ℃时,现象如图乙所示。KNO3和NaCl的溶解度曲线如图丙。请回答下列问题:
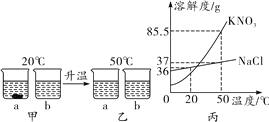
(1)a烧杯中加入的物质是______(填化学式)。
(2)甲图中,a烧杯溶液中溶质的质量分数______(“>”、“<”或“=”)b烧杯溶液中溶质的质量分数。
(3)要使乙图中的NaCl溶液恰好变成饱和溶液,需要加入________g NaCl固体。
(4)除去NaCl固体中混有的少量KNO3,实验步骤:先加水溶解,再________,然后过滤、洗涤、干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法正确的是( )
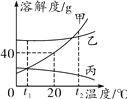
A. t2℃时,三种物质的溶解度:乙>甲>丙
B. 20 ℃时,将30 g甲放入50 g水中,充分搅拌,所得溶液的质量是80 g
C. 分别将t2 ℃时三种物质的饱和溶液降温到t1℃,乙溶液中析出的固体质量最大
D. 分别将t1 ℃时三种物质的饱和溶液升温到t2℃,溶液中溶质的质量分数:乙>甲>丙
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答下列问题。
(1)用化学用语表示:
①氯化钠中的阳离子__________;②硫酸亚铁中铁元素的化合价__________。
③氯气(Cl2)是一种重要工业原料,实验室通常以二氧化锰和浓盐酸制备氯气,发生如下反应:MnO2+4HCl(浓) ![]() Cl2↑+X+2H2O,其中X的化学式是__________。
Cl2↑+X+2H2O,其中X的化学式是__________。
④氢气是清洁能源,其燃烧的化学方程式为__________。
(2)铁是应用最广泛的金属。
①喷漆能防止铁生锈,原因是__________。
②工业炼铁时,一氧化碳和赤铁矿(主要成分是氧化铁)发生的主要反应的化学方程式为__________。
(3)水是生命之源。
①生活中既能降低水的硬度,又能杀菌消毒的方法是__________。
②含氮的物质进入水中会造成水中藻类大量繁殖,使水体富营养化,导致水质恶化。这里的“氮”是指__________(填序号)。
A.元素 B.原子 C.离子 D.分子
查看答案和解析>>
科目: 来源: 题型:
【题目】“冰毒”是毒性极强的毒品之一,其化学式为C10H15N,下列有关冰毒解释错误的是( )
A.冰毒是由碳、氢、氮三种元素组成的化合物
B.冰毒是一种有机物,完全燃烧只生成CO2和H2O
C.冰毒中氮原子的原子结构示意图为![]()
D.冰毒中碳、氢两种元素质量比为24:3
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种常见固体物质的溶解度曲线,下列说法正确的是

A. t2℃时,物质甲的饱和溶液的溶质质量分数为50%
B. t1℃时,甲、丙的饱和溶液中溶质与溶液的质量比均为1∶5
C. 除去乙物质中少量甲物质可采取降温结晶的方法
D. 将甲、乙的饱和溶液分别从t1℃升温到t2℃,溶质质量分数都不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com