
科目: 来源: 题型:
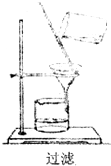 晓刚有一杯松花江水样品,浑浊且有异味,请你用学过的知识帮助他除去其中的不溶物和异味.
晓刚有一杯松花江水样品,浑浊且有异味,请你用学过的知识帮助他除去其中的不溶物和异味.查看答案和解析>>
科目: 来源: 题型:
| 实验编号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸的用量 | 5g | 5g | 5g | 5g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 盐 酸 体积:500mL 化学式:HCl 相对分子质量:36.5 密度:1.19g/cm3 质量分数:37%(1)瓶内浓盐酸的质量是 (2)用10mL浓盐酸可以配制溶质的质量分数为10%的盐酸溶液 查看答案和解析>> 科目: 来源: 题型: 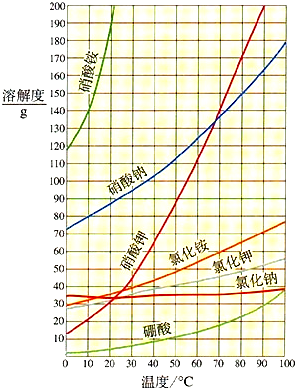 126g溶质质量分数为10%的硝酸溶液与91g氢氧化钠溶液恰好完全反应,试计算: 126g溶质质量分数为10%的硝酸溶液与91g氢氧化钠溶液恰好完全反应,试计算:(1)生成硝酸钠 (2)原氢氧化钠溶液中溶质的质量分数是 (3)根据如图分析计算,若要形成10℃时硝酸钠的饱和溶液,可用 查看答案和解析>> 科目: 来源: 题型: 根据下列装置图回答问题: 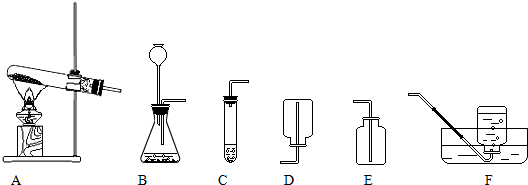 (1)实验室用高锰酸钾制取氧气,选用的气体发生装置为 (2)实验室用大理石和稀盐酸制取二氧化碳,选用的气体发生装置为 查看答案和解析>> 科目: 来源: 题型: 为了对海水中的氯化物(假设以NaCl计算)进行成分分析,甲、乙、丙三位同学分别进行实验,他们的实验数据如下.请仔细观察分析,回答下列问题.
(2)海水中氯化物(以NaCl计算)的质量分数是多少? 注:反应的化学方程式为:NaCl+AgNO3═AgCl↓+NaNO3. 查看答案和解析>> 科目: 来源: 题型: 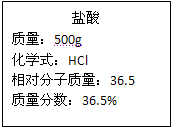 实验室有一瓶浓盐酸,瓶上标签的部分内容如图所示,请你根据标签上提供的数据解答下列问题: 实验室有一瓶浓盐酸,瓶上标签的部分内容如图所示,请你根据标签上提供的数据解答下列问题:(1)为了证明该瓶盐酸显酸性,你可以采取的做法是 (2)取出200g该浓盐酸,稀释成18.25%的稀盐酸,需要加入水的质量为 (3)现用刚配好的100g 18.25%的盐酸与足量的锌粒完全反应,理论上可以生成氢气的质量是多少?(反应化学方程式:Zn+2HCl=ZnCl2+H2↑) 查看答案和解析>> 科目: 来源: 题型: 现有Cu与另一种金属(可能是Mg、Fe、Zn中的一种)形成的粉末.现欲测定其组成,进行如下实验:取该粉末16g放入烧杯,将溶质质量分数为14%的稀硫酸280.0g分4次加入该烧杯中,充分反应后,测得剩余的固体质量数据记录如下:
(1)该粉末中Cu的质量分数. (2)该粉末中另一种金属为何种金属. (3)第3次加入稀硫酸充分反应后,所得溶液中溶质的质量分数. 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |