
科目: 来源: 题型:阅读理解
小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%。小明想,这瓶白醋中醋酸的含量是否与标签的标注相符?请你与小明一起,用有关化学知识,定量测定白醋中醋酸的含量。
【提出问题】这瓶白醋中醋酸的含量是否与标签的标注相符?
【实验原理】
(1)醋酸属于 __ (“有机”或“无机”)酸,能与 ____ (填物质类别)发生中和反应。
(2)用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:
CH3COOH + NaOH = CH3COONa + H2O。
(3)在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05 mL,对测定结果的影响很小,可忽略不计。
【实验步骤】
(1)用 取10.0 mL白醋(密度近似为1.0g/ mL),倒入烧杯中,再加入20 mL蒸馏水稀释。
(2)量取45.0 mL溶质质量分数为1.0%的氢氧化钠溶液(密度近似为1.0 g/ mL),用胶头滴管吸取该氢氧化钠溶液,逐滴地滴加到稀释后的白醋中,同时不断地搅拌烧杯中的溶液。滴至恰好完全反应,剩余氢氧化钠溶液5.0 mL。
【交流反思】
(1)在实验步骤(1)中,加适量水稀释白醋,对实验结果 (“有”或“无”)影响?为什么? 。
(2)在实验步骤(2)中,小明如何确定醋酸和氢氧化钠已完全中和?
| 实验操作 | 实验现象 | 结论 |
【解释与结论】
根据实验数据,通过计算,判断这瓶白醋中醋酸的含量 (“是”或“否”)与标签的标注相符。
查看答案和解析>>
科目: 来源: 题型:
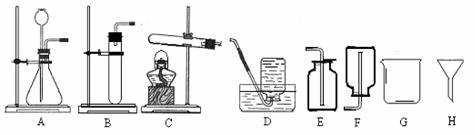 请你根据下图回答下列问题:
请你根据下图回答下列问题:
(1)指出下列编号仪器的名称:G 、H ;
(2)实验室用氯酸钾和二氧化锰混合加热制取氧气时可选用的发生装置是 ,可以选用的收集装置是 ;
 (3)硫化氢是一种有毒气体,其密度比空气大,易溶于水,它的水溶液叫氢硫酸。实验室通常用块状固体硫化亚铁(FeS)与稀硫酸在常温下反应制取硫化氢气体,制取气体的发生装置是 。请在右边方框中补画出收集硫化氢气体的装置并用箭头表示气体的进出方向。
(3)硫化氢是一种有毒气体,其密度比空气大,易溶于水,它的水溶液叫氢硫酸。实验室通常用块状固体硫化亚铁(FeS)与稀硫酸在常温下反应制取硫化氢气体,制取气体的发生装置是 。请在右边方框中补画出收集硫化氢气体的装置并用箭头表示气体的进出方向。
(4)收集气体后,为防止多余的硫化氢气体逸出到空气中,应采取的措施是 。
查看答案和解析>>
科目: 来源: 题型:
有一种碳酸盐的矿石,其主要成分为BaCO3和CaCO3,这两种盐有相似的性质,如:都难溶于水;高温煅烧都可以分解成为氧化物;都能与二氧化碳和水反应,生成可溶性的盐。钡和钙元素的氧化物和氢氧化物也有相似的化学性质,但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度。
|
溶解度/g 物质 | 0 | 40 | 80 |
|
| 0.187 | 0.141 | 0.094 |
|
| 1.67 | 8.22 | 101.4 |
为除去矿石中的CaCO3得到较纯净的BaCO3,某同学根据上述信息,对矿石样品进行了如下图所示的四步处理。
![]()
(1)写出实现上图各步转化过程中的实验方法(分别填写反应条件、所加试剂、操作方法等)。
① ② ③ ④
(2)写出第②步发生反应的化学方程式:
② ; 。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组取一小块红色石块A,粉碎后对其成分进行实验探究,实验记录如下图所示。
请你根据实验推断:A中含有的原子团是 (写离子符号)。
B中肯定含有的溶质是 (写化学式)。
写出实验中有关反应的化学方程式:②
⑤ 
查看答案和解析>>
科目: 来源: 题型:
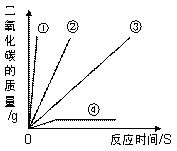
为了选择实验室制取二氧化碳的反应物,某实验小组取等量的碳酸盐和足量等浓度的酸,设计了以下四种反应物组合进行探究实验,结果如下图所示。
|
(1)根据实验结果,他们决定选择大理石与稀盐酸来制取二氧化碳,他们不选择①和④的原因分别是_______________ ___ ; 。
(2)探究结果说明,影响碳酸盐与酸反应产生二氧化碳快慢的因素有_______________
_______________________ 。(有几点写几点)
查看答案和解析>>
科目: 来源: 题型:
某盐水主要是含氯化钠,此外还含有较多硫酸钠,以及少量的氯化钙和氯化镁。
上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(1)在同温下,溶解度最大的物质是_______。
(2)根据所提供的溶解度数据,画出氯化镁的溶解度曲线;
 |
(3)从溶液中获得硫酸钠晶体适宜采用_________________的方法。
(4)30℃时,100g氯化钙饱和溶液中,氯化钙的质量为_____g。
查看答案和解析>>
科目: 来源: 题型:
课外小组的同学研究的课题是测定贝壳中碳酸钙的质量分数,他们取25g贝壳粉碎后放入烧杯中,向杯中倒入稀盐酸,当倒入100g稀盐酸后发现不再产生气泡,并测得烧杯内固体和液体总质量为120.6g (杂质不反应)。求贝壳中碳酸钙的质量分数。
查看答案和解析>>
科目: 来源: 题型:
在研究酸雨的危害时,进行如下探究:
[提出问题]酸雨能腐蚀自然界中的哪些物品呢?
[设计实验]实验1:如图,硫在氧气中燃烧,观察到的现象是_______________________,实验中出现的错误是__________________________。

若按正确操作,反应后向瓶中倒入蒸馏水,振荡,使SO2与水反应生成亚硫酸H2SO3,一段时间后,亚硫酸与氧气反应生成硫酸,有关方程式为:_________________________、 。
实验2:将所得硫酸型酸雨溶液分成三等分,分别向其中加入如下物质,并观察到如下现象:
| 所得溶液 | 加入的物质 | 一段时间后,观察到的现象 |
| 1份 | 植物树叶和果皮 | 树叶和果皮被腐蚀 |
| 2份 | 镁条和铁丝 | 有气泡产生 |
| 3份 | 石灰石和水泥残片 | 有气泡产生 |
[反思与交流](1)酸雨不仅能腐蚀大理石雕像(如图),还能腐蚀_________________________,有同学提出制取CO2时,不能用大理石和稀硫酸反应,为什么硫酸型酸雨能腐蚀大理石雕像呢?你认为原因是___________________________。

(2)土壤中有许多细小的石子,有人说酸雨还能加剧“温室效应”,这种说法的依据是:
___________________________________________。
[拓展与应用]怎样防治酸雨产生,请你提出两点建议:
①____________________________; ②_____________________________。
查看答案和解析>>
科目: 来源: 题型:
右图是教材中有关《质量守恒定律》的实验,试回答下列问题:

(1)反应中观察到的现象是
________________________________________________ ;
(2)左盘锥形瓶口在白磷点燃后要塞紧瓶塞,原因是
;
(3)在实验设计上,玻璃管上方系一瘪气球的目的是
________________________________________________________________________;
(4)实验结束后(锥形瓶已冷却到室温),发现瓶中白磷过量,为了防止白磷在空气中燃烧,将锥形瓶瓶口倒置于盛满水的水槽中(如图,瓶口贴紧水面),拔下瓶塞, 发现水进入锥形瓶中,则进入瓶中的水占锥形瓶的容积的 ,原因是: 。
![]()
查看答案和解析>>
科目: 来源: 题型:
实验室有下列仪器和高锰酸钾、氯酸钾、石灰石、二氧化锰、稀盐酸五种药品及木块、火柴等实验用品。某同学想利用这些仪器和药品制取某种常见的气体,请回答下列问题:
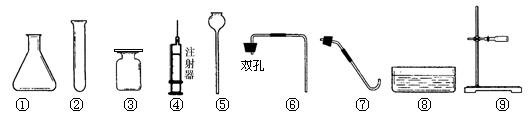
(1)用氯酸钾法制取气体时,缺少的仪器是______,用高锰酸钾制取气体时不仅缺少上述提到的仪器,还缺少用品________,没有这种用品会引起的后果是_________________;
(2)利用上述仪器和药品制取大量的某种常见气体,在制取时并能控制反应的速率,选用的仪器是__________________(填标号)。(2分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com