
科目: 来源: 题型:
“低碳经济,低碳生活”内涵之一是减少二氧化碳的排放,已成为社会发展和家庭生活的主流。下列行为不符合“低碳”理念的是 ( )
A.为提高生活水平,大量使用空调、电热水噐、电磁炉、冰箱、电视机等电器
B.发展太阳能、风能等新能源
C.近距离出行时,用自行车替代机动车
D.研制、推广使用以氢气、氧气提供动力的客车
查看答案和解析>>
科目: 来源: 题型:
已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首。
(1)据此推断X是 (填选项字母)。
A.钛 B.铁 C.铝 D.铜
(2)在高炉中用含X2O3的矿物冶炼该金属的原理是
(用化学方程式表示)。
(3)同学们设计了如下实验方案测定该矿物中X2O3的质量分数(装置气密性良好;矿物中的杂质不参加反应;假设矿物样品中的X2O3完全反应):
①取矿物样品并称量该样品的质量;
②测出反应前广口瓶和瓶内物质总质量;
③测出反应后广口瓶和瓶内物质总质量;
④计算得出矿物样品中x2O3的质量分数。你认为,该实验方案 (填“一定”
或“不一定”)能准确测出矿物中X2O3的质量分数,理由是
。
不改变装置和药品,你还可以通过测定哪些数据,再通过计算得出矿物中X2O3的质量分数:
。
从环保角度看,该装置的不足之处是 。
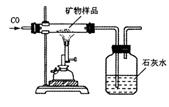
查看答案和解析>>
科目: 来源: 题型:
利用废铜屑制硫酸铜,有两种方案:
①Cu+2H2SO4(浓) ![]() CuSO4+X↑+2H2O
CuSO4+X↑+2H2O
②2Cu+O2 ![]() 2CuO,CuO+ H2SO4
2CuO,CuO+ H2SO4 ![]() CuSO4+ H2O。回答下列问题:
CuSO4+ H2O。回答下列问题:
(1)X是 (写化学式)。
(2)你认为较好的方案是 (填“①”或“②”),其优点有 。
查看答案和解析>>
科目: 来源: 题型:
今年上海世博会中国国家馆,由于形状酷似一顶古帽,被命名—“东方之冠”,给人强烈的视觉冲击。“东方之冠”的主体结构为四根巨型钢筋混凝土制成的陔心筒。根据你所学的化学知识回答:(1)钢筋属于 材料,其主要成分是铁,写出铁的化学式: 。
(2)被混凝土严密包裹的钢筋不易生锈的原因是 。
(3)对废旧钢筋进行回收利用的目的是 (填“合理开采矿物”或“节约金属资源”)。
查看答案和解析>>
科目: 来源: 题型:
为探究铁锈蚀的影响因素,某兴趣小组做了如下实验。
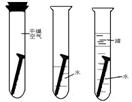
[实验方案] 将3枚洁净的铁钉同时置于如图所示环境下的斌舒中,观察铁钉锈蚀情况。
[实验现象]3天后,I、Ⅲ中铁钉不生锈,Ⅱ中铁钉明显生锈。
[获得结论]
(1)对照实验l、Ⅱ,可知铁锈蚀的条件之一为 ;
(2)防止铁锈蚀的一种方法是 。
[拓展探究]
(3)小明发现海边的铁器很容易生锈,从而猜测氯化钠能加快铁的锈蚀。请设计实验方案验证小明的猜想 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
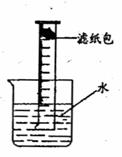
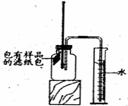
小明对铁的锈蚀进行如下探究。室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图。观察到量筒内水沿导管慢慢进入广口瓶(净容积为146 mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如下表.
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1 g铁粉、0.2 g碳和10滴水 | 100 | 70 | 约120 |
| ② | l g铁粉、0.2 g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
| ③ |
(1)实验①和②说明NaCl可以 (填“加快”或“减慢”)铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是 (填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是 。
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是 %(保留3位有效数字)。
注意:若答对第(6)小题将奖励4分。但化学试卷总分不超过60分。
(6)现仅提供:置筒、大烧杯、玻璃棒、水、滤纸包(内含1 g铁粉、O.2 g碳、10滴水和少量NaCl),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,在右框中画出实验装置示意图即可(注明滤纸包的位置)。

查看答案和解析>>
科目: 来源: 题型:
人类每年都要从大自然中提取大量的金属,用于满足日常生活和工农业生产的需要。
(1)钢铁是我们日常生活中使用最多的金属材料。高炉炼铁常以焦炭、铁矿石、石灰石、空气等为原料。炼铁过程中,一氧化碳和赤铁矿(主要成分为Fe2O3)反应的化学方程式为 。
(2)我国钢铁年产量很高,但因锈蚀造成的损失也很惊人。人们常采取在铁制品表面涂刷油漆或镀上其他金属等方法,以防止其锈蚀。上述方法所依据的原理是 。
(3)我国矿物储量很丰富,但人均占有量并不多,请保护金属资源!下面几种做法中,可有效保护金属资源的是 (填字母)。
a.回收利用废旧金属制品
b.任意开采铁矿石
c.铁制品不加处理,存放在潮湿的环境中
d.寻找、开发金属的代用品
查看答案和解析>>
科目: 来源: 题型:
铁、铝、铜市日常生活中使用最广泛的金属。
(1)上述三种金属中,人类最早大规模冶炼和使用的是铜,最晚的是铝,原因是 (填序号)。
A. 三者在地壳中的含量,铜元素最高,铝元素最低
B. 三者的金属活动性,铜元素最弱,铝元素最强
C. 在自然界中,铜元素主要以单质形式存在,铝元素以化合物形式存在。
(2)常温下一些金属的物理性质数据如下:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g·cm3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5-3 | 2-2.9 | 2.5 | 4-5 | 1.5 |
分析上述数据,碎石用的大锤常用铁制而不用铝制,原因是
(3)铜器长期暴露在空气中,表面会生成铜绿,其成分可表示为Cu2(OH)2CO3,从其组成分析,预测铜绿能与 (任举一例)反应。
(4)工业上火法炼铜的一个主要反应是Cu2S+O2![]() 2Cu+SO2。Cu2S中铜元素的质量分数为 。用500吨含Cu2S80%的铜矿石,理论上可以炼出 吨铜。
2Cu+SO2。Cu2S中铜元素的质量分数为 。用500吨含Cu2S80%的铜矿石,理论上可以炼出 吨铜。
查看答案和解析>>
科目: 来源: 题型:
汽车使用是人类进步的标志,但生产汽车的材料、使用的能源等是人们关注并需解决的问题。
(1)制造汽车的材料以钢铁为主,钢是铁和 的合金;写出在高温下一氧化碳与氧化铁反应的化学方程式 。
(2)钢铁的防腐是汽车制造业研究的重要课题之一。铁生锈的原因是 。
 (3)有些汽车新型排气系统中,使用抗腐蚀性能好的钛合金材料。生产钛(Ti)的部分工艺流程图如下:
(3)有些汽车新型排气系统中,使用抗腐蚀性能好的钛合金材料。生产钛(Ti)的部分工艺流程图如下:
回答下列问题:
① 二氧化钛中钛元素的化合价为 价。
② 写出镁与四氯化钛(TiCl4)发生反应的化学方程式 ;该反应类型属于 。上述反应需在氩气环境中进行,理由是 。
(4)家用汽车和公交车相比,前者的耗油量大约是后者的1/5左右。前者和后者在行驶时所排出的污染物的比率大致也是1/5左右。 如果后者载运乘客量平均为50人,前者平均为2人,请对比它们在燃料利用和污染环境方面因素,你的建议是 。
查看答案和解析>>
科目: 来源: 题型:
(1)磁铁矿的主要成分是: ;(填化学式)
(2)写出CO与Fe2O3在高温条件下反应的化学方程式: ;
(3)高炉炼铁得到的主要产品是 ;(填序号)
A.纯铁 B.生铁 C.钢
(4)铁生锈的主要条件是铁与水和 直接接触。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com