
科目: 来源: 题型:
(6分)化学与生产、生活密切相关。
⑴高岭土是制造瓷器的一种主要原料,其主要成分是一种硅酸盐[化学式为Al2(Si2O5)(OH)4]。这种硅酸盐中含有的非金属元素有 ▲ 种。
⑵夏天用来清凉散热、醒脑提神的清凉油主要成分为薄荷脑(化学式为C10H20O)。该物质中碳元素和氢元素的质量比为 ▲ 。
⑶将辰砂和铁粉的混合物加热,生成了汞和硫化亚铁,由此推测辰砂中一定含元素▲ 。
⑷“蜂窝煤”被加工成多孔形状的原因是 ▲ 。制作“蜂窝煤”时常加入生石灰(主要成分为氧化钙),其燃烧过程发生的部分化学反应如下:①SO2 + CaO 高温 CaSO3,
②2CaSO3 + O2 高温 2CaSO4,③2SO2 + O2 高温 2SO3,④SO3 + CaO 高温 CaSO4。上述反应属于 ▲ 反应(填基本反应类型);制作“蜂窝煤”时加入生石灰的作用 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(5分)根据下图回答问题。
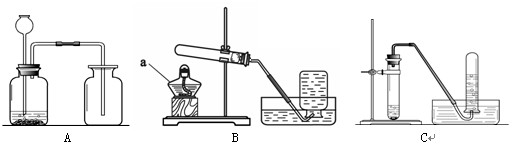
⑴仪器a的名称为 ▲ 。
⑵加热高锰酸钾制取氧气的装置是 ▲ (填序号),反应的化学方程式为 ▲ 。
⑶根据CO2的性质分析,制备二氧化碳气体的装置选用A而不选用C的原因是 ▲ ,
检验二氧化碳已经收集满的方法是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(5分)过氧化钠(化学式为Na2O2)能与CO2反应,化学方程式为2Na2O2 + 2CO2 = 2Na2CO3 + O2↑,可用在呼吸面具中作为氧气来源。某实验小组欲用干燥的二氧化碳与过氧化钠反应收集一瓶氧气,实验装置如下图所示,请回答问题。
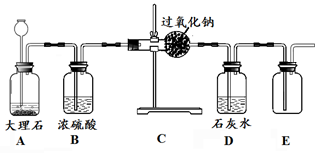
⑴实验室制取二氧化碳的化学方程式为 ▲ 。
⑵浓硫酸的作用是 ▲ 。
⑶若实验过程中发现澄清的石灰水变浑浊,其原因可能为 ▲ ,发生反应的化学方程式为
⑷氧气可用E装置收集,并用带火星的木条检验,这是利用了氧气的 ▲ 性质
查看答案和解析>>
科目: 来源: 题型:
(9分)已知某金属粉末中可能含有铁、铝、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究。
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由 ▲ 组成。
【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al + 2H2O + 2NaOH = 2NaAlO2 + 3H2↑,铁和铜与氢氧化钠溶液均不发生反应。
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水。
【进行实验】
| 实验目的 | 实验操作 | 实验现象 | 实验结论 |
| 证明粉末中是否含有 ▲ | 取一个小烧杯,加入适量的粉末,再向其中加入足量的 ▲ |
▲ |
猜想四成立; 实验中发生反应 的化学方程式为 ▲ |
| 证明粉末中是否含有 ▲ | 过滤,将得到的固体洗涤后放入小烧杯,再向其中加入足量的稀盐酸 |
▲ |
【反思与评价】若将原粉末中的铜全部回收,请写出实验过程 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(3分)氢化钙(CaH2)是一种重要的制氢剂,与水接触时发生反应的化学方程式为CaH2 + 2H2O =Ca(OH)2 + 2H2↑。若制取10 g氢气,需要消耗多少氢化钙?
查看答案和解析>>
科目: 来源: 题型:
(3分)为测定某碳酸钠样品(其中杂质不溶于水)纯度,进行了以下实验:取48 g样品加入水使碳酸钠完全溶解后除去杂质,将得到的液体平均分为四份,每份中分别加入一定质量的氯化钙溶液,反应的化学方程式为CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl,实验数据见下表。
|
| 第一份 | 第二份 | 第三份 | 第四份 |
| 加入CaCl2溶液的质量/g | 10 | 20 | 30 | 40 |
| 生成沉淀的质量/g | 4 | 8 | 10 | 10 |
请计算:
⑴每份液体完全反应时,生成沉淀的质量为 ▲ g。
⑵样品中碳酸钠的纯度。
查看答案和解析>>
科目: 来源: 题型:
武广高速全程都是无缝铁轨。显然,无缝铁轨不可能一次成型,无缝铁轨是在铺设时将短轨通过如下反应原理:2Al+Fe2O3Al2O3+2Fe焊接而成。该反应是( )
A.复分解反应 B.置换反应 C.分解反应 D.化合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com