
科目: 来源: 题型:
阳光牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水。使用一段时间后,其中的Fe粉会转变成Fe2O3而变质。某化学兴趣小组欲探究使用过的阳光牌“脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行如下探究过程。
步骤①:取食品包装袋中的阳光牌“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣。
步骤②:取步骤①中的滤渣8.0 g,加入足量的稀H2SO4与滤渣充分反应,过滤、洗涤、干燥得固体1.2 g。
步骤③:取步骤②中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0 g Fe2O3(注:滤液中的Fe元素已全部转化为Fe2O3)。求:
(1) 8.0g滤渣中Fe和Fe2O3两种物质的总质量。
(2)该“脱氧剂”在未变质时,Fe粉和活性炭的质量之比。
(3)该“脱氧剂”的变质程度。
查看答案和解析>>
科目: 来源: 题型:
NaOH潮解后极易与空气中的CO2反应生成Na2CO3而变质。为测定实验室一瓶放置已久的烧碱中NaOH的含量,某同学取适量的烧碱样品,溶于一定量的水得到200 g溶液;再加入200 g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g。请计算:
(1)反应产生的CO2的质量为_______g。
(2)若所取烧碱样品为50.0 g,则样品中NaOH的质量分数是多少?
(3)用同浓度的硫酸,与一瓶未变质、部分变质、全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等。其原因是_______(从钠元素质量守恒的角度解释)。
查看答案和解析>>
科目: 来源: 题型:
某课外活动小组为了测定一批石灰石中碳酸钙的质量分数,将石灰石样品研成粉末,然后取一定量的石灰石粉末与过量稀盐酸充分反应(假设石灰石中的杂质既不和酸反应,也不溶于水),过滤、洗涤、干燥后称量滤渣质量的数据如下表:
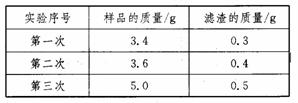
(1)该样品中碳酸钙质量分数的平均值为_______(结果精确到0.1%)。
(2)引起三次实验数据差异的操作原因可能是_______.
(3)若利用题(1)的结果,煅烧100 t这种石灰石,理论上最多能得到氧化钙多少吨?(结果精确到0.1 t)
查看答案和解析>>
科目: 来源: 题型:
利用下图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化).实验数据记录在下表中。
提示:FeCO3 FeO+CO2↑。
FeO+CO2↑。

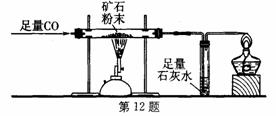
(1)该含菱铁矿的矿石样品中碳酸亚铁的质量分数为_______。
(2)实验结束后盛有澄清石灰水的试管的总质量比反应前的总质量增加了_______g。
查看答案和解析>>
科目: 来源: 题型:
乙醇(化学式:C2H5OH)是一种能替代汽油等燃料的清洁能源,但在氧气不足时燃烧除生成二氧化碳和水外,还会生成一氧化碳。现有69 g乙醇与一定量的氧气点燃后发生如下反应:xC2H5OH+8O2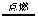 yCO2+zCO+9H2O。
yCO2+zCO+9H2O。
(1)判断x的值是_______。
(2)计算反应后生成一氧化碳的质量。
查看答案和解析>>
科目: 来源: 题型:
在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50 g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质.充分反应后,天平发生偏转的是( )
A.1.8g铝粉和1.8 g铁粉 B.4.2g碳酸镁和2g硝酸银
C.5.6g铁粉和5.6g锌粉 D.7.8g碳酸钙和5.6 g氧化钙
查看答案和解析>>
科目: 来源: 题型:
某固体样品中除了含有在高温下不分解,也不与空气成分反应的物质外,还可能含有CaCO3、CaO中的一种或两种。某化学兴趣小组为探究该固体的成分,称量样品m1 g,经高温充分煅烧并在干燥的保护气中冷却,至质量不再减轻为止,剩余固体的质量为m2 g。下列推断不正确的是 ( )
A.若m1=m2,则原样品中无CaCO3
B.若m2<m1,则原样品中一定有CaCO3
C.若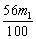 <m2<m1,则原样品中一定有CaO
<m2<m1,则原样品中一定有CaO
D.若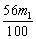 <m2<m1,则原样品中一定无CaO
<m2<m1,则原样品中一定无CaO
查看答案和解析>>
科目: 来源: 题型:
已部分变质的Ca(OH)2固体试样10 g,与足量稀盐酸反应,产生2.2 g CO2,则该固体中Ca(OH)2的质量分数为 ( )
A.30% B.40% C.50% D.60%
查看答案和解析>>
科目: 来源: 题型:
在托盘天平的左、右两盘中各放一只烧杯,调节至平衡,向烧杯分别注入等质量、质量分数相同的稀硫酸,然后向两只烧杯中分别加入相同质量的铜铝合金和锌,待物质反应结束后,天平仍保持平衡,合金中铝与铜的质量比为 ( )
A.18:47 B.54:65 C.27:64 D.27:38
查看答案和解析>>
科目: 来源: 题型:
物质R在0. 96 g氧气中恰好完全燃烧,反应的化学方程式为:R+3O2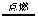 XO2+2SO2,测得XO2和SO2的质量分别为0.44 g和1.28 g。下列判断正确的是 ( )
XO2+2SO2,测得XO2和SO2的质量分别为0.44 g和1.28 g。下列判断正确的是 ( )
A.参加反应的R的质量为0.86 g
B.R的相对分子质量为76
C.R中含有X元素、S元素和O元素
D.XO2和SO2都是形成酸雨的主要物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com