
科目: 来源: 题型:
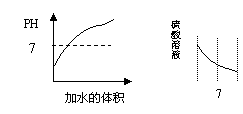
下列四个图像分别表示对应的四种操作过程,其中表示正确的图像是 ( )


|
|
|
|
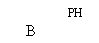 | |||||||
| |||||||
| |||||||
| |||||||
A.向pH=1的酸溶液中不断加水
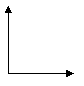
B.向pH=1的硫酸溶液中逐滴加入pH=13的氢氧化钠溶液
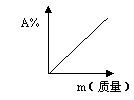
C.某温度下,向一定量的水中持续加入食盐并不断搅拌 (m表示加入食盐的质量,A%表示溶质质量分数)
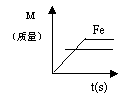
D.等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量M与反应时间t的关系图
查看答案和解析>>
科目: 来源: 题型:
推理是学习化学的一种方法,但不合理的推理会得到错误结论。以下推理正确的是( )
A.分子可以构成物质——物质一定由分子构成
B.溶液具有均一性和稳定性——具有均一性、稳定性的液体一定是溶液
C.含碳元素的物质燃烧会生成二氧化碳——燃烧能生成二氧化碳的物质一定含有碳元素
D.化学反应常常伴随着能量变化——有能量释放的变化都是化学反应
查看答案和解析>>
科目: 来源: 题型:
某反应的微观示意图如下,下列说法正确的是 ( )
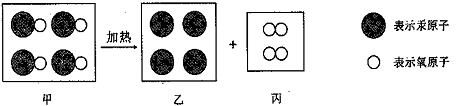
A. 图中甲、乙、丙三种物质均是由分子构成的
B. 图中甲、乙、丙三种物质中,甲、丙属于氧化物
C. 该反应前后分子种类、原子种类均没有改变
D. 图中甲、乙、丙三种物质既有单质又有化合物
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
A.可燃物达到着火点一定会燃烧
B.干冰升华时要吸收大量的热,这是化学变化中的吸热现象
C.某气体能使灼热的氧化铜还原成铜,这种气体一定是一氧化碳
D.鉴别氢氧化钠固体和氯化铵固体,可加适量水溶解,用手触摸试管外壁温度的变化
查看答案和解析>>
科目: 来源: 题型:
为了测定某粉末状黄铜(铜锌合金)样品中铜的质量分数,洋洋同学取一定质量的黄铜样品放入烧杯中,再取40 g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 9.10 | 8.45 | 7.80 | 7.80 |
(1)上述反应的化学方程式为________________________;
(2)根据锌的质量列出求解第二次生成氢气质量(x)的比例式________________;
(3)所用稀盐酸中溶质的质量分数为________;
(4)用36.5%的浓盐酸配制40 g上述稀盐酸,需要浓盐酸的质量为________;
(5)黄铜样品中铜的质量分数为__________。
查看答案和解析>>
科目: 来源: 题型:
我国某地区有一种“冬天捞碱,夏天晒盐”的说法,这里的“碱”是指Na2CO3,“盐”是指NaCl。这样捞得的“碱”中含有少量NaCl。某化学课外活动小组为了解释捞碱、晒盐的原理和测定“碱”样品中Na2CO3的含量进行了以下探究。
[查阅资料]
Na2CO3和NaCl的溶解度曲线如图所示。
(1)根据图示回答:①t1 ℃时Na2CO3的溶解度为________ g;t2 ℃时Na2CO3的溶解度________(填“>”“=”或“<”)NaCl的溶解度。
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度的降低而________(填“增大”“减小”或“不变”)。
③“夏天晒盐”是利用________(填字母)的方法,使NaCl晶体析出。

A.利用风吹日晒,使溶剂蒸发 B.升高温度,使NaCl的溶解度增大
[实验步骤]
第一步:称取34.6 g“碱”样品。
第二步:将该样品放入13 0 g稀盐酸中,两者恰好完全反应。其化学方程式为Na2CO3+2HCl===2NaCl+H2O+CO2↑
0 g稀盐酸中,两者恰好完全反应。其化学方程式为Na2CO3+2HCl===2NaCl+H2O+CO2↑
第三步:完全反应后,称得溶液的总质量为151.4 g,经计算可知释放出的二氧化碳的质量为13.2 g。
[数据分析]
(2)试计算:(结果保留一位小数)
①Na2CO3的相对分子质量。②34.6 g“碱”样品中碳酸钠的质量。③“碱”样品中Na2CO3的纯度。
[继续探究]
(3)计算反应后所得溶液中NaCl的质量分数。
查看答案和解析>>
科目: 来源: 题型:阅读理解
在日常生活中,我们发现切过咸菜的刀更容易生锈,而除锈用稀盐酸比稀硫酸快。为了进一步验证上述现象,某校师生做了以下相关分组实验,请你根据自己平时课堂学习的体验一起参与讨论并回答相关问题。
【步骤一】未打磨的铝片浸入氯化铜溶液中,迅速产生大量气泡和疏松的紫红色固体,并放热,片刻后溶液由蓝绿色变成无色。
(1)若要验证紫红色固体中是否含有氧化铜,可用________(填一试剂)加以检验。
【步骤二】未打磨的铝片浸入硫酸铜溶液中,一段时间内没有明显现象。
(2)比较步骤一、二,你能得出的结论是__________________________。
【步骤三】打磨过的铝片浸入硫酸铜溶液中,其操作、现象和结论见下表。
(3)试将下表“影响因素”选项前恰当的字母序号填入指定位置。
| 实验操作 | 实验现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 现象二:粗砂纸打磨的片刻内现象不明显。 | 现象一与现象二对比,说明: ①____________ |
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象三与现象一对比,说明:②________;现象四与现象三对比,说明:③__________ |
★影响因素:
A.打磨时用力程度及均匀程度不同 B.选用砂纸颗粒粗细程度不同
C.由于摩擦生热又形成了新的氧化膜
(4)比较步骤三各实验操作中用砂纸打磨的作用是______________________________。
(5)请仔细观察下图。
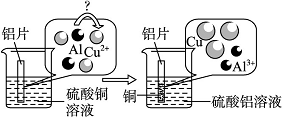
试从微观粒子变化的角度分析该反应的实质:_______________________________。
查看答案和解析>>
科目: 来源: 题型:
海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富的化学资源。某市具有较长的海岸线,海洋资源开发前景广阔。
(1)目 前海水淡化普遍采用的方法是____________________,证明得到的水是淡水的方法是________________________。
前海水淡化普遍采用的方法是____________________,证明得到的水是淡水的方法是________________________。
(2)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型资源是____________________,被科学家誉为“21世纪能源”。
(3)海水晒盐能够得到粗盐和卤水。
①卤水中含有MgCl2、KCl和MgSO4等物质,下图是它们的溶解度曲线。t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是__________。
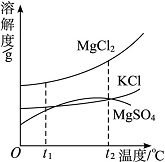
②将粗盐提纯可以得到纯净的NaCl。欲用纯净的NaCl配制100 g 0.9%的生理盐水,需要NaCl的质量为__________ g。配制该溶液时需要的玻璃仪器有_____________________。如果配制的溶液的溶质质量分数低于0.9%,你认为可能的原因是____________________(任写一个)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com