
科目: 来源:2011-2012学年天津市宝坻八中九年级结课考试化学试卷(带解析) 题型:计算题
(4分)2007年9月2日,河南省清流县一载满浓硫酸的罐车翻倒,导致26 t溶质质量分数为98%的浓硫酸泄漏,流入附近小溪中。闻讯赶来的武警官兵立即垒坝并用石灰浆(主要成分是氢氧化钙)中和硫酸。计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙?
查看答案和解析>>
科目: 来源:2012届江苏省南京市第三初级中学九年级课程结束考试化学试卷(带解析) 题型:计算题
请根据下图所示的实验过程和提供的数据,计算样品中钠元素的质量。 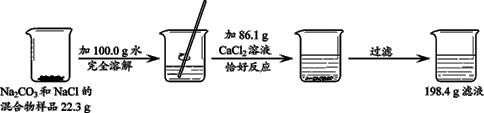
▲(写出计算过程)
查看答案和解析>>
科目: 来源:2012届江苏省丹阳市司徒中学九年级下学期第一次质量检测化学试卷(带解析) 题型:计算题
(4分)将一定量10 %的氯化钙溶液与一定量10 %的碳酸钠溶液混合,恰好完全反应,反应后过滤得难溶固体5g ,若将滤液蒸发去45g水,求所得溶液中溶质的质量分数。
查看答案和解析>>
科目: 来源:2012届江苏省丹阳市司徒中学九年级下学期第一次质量检测化学试卷(带解析) 题型:计算题
(9分)某纯碱样品中含有少量氯化钠,现欲测定其中碳酸钠的质量分数,进行如下实验:
《实验原理》:Na2CO3+H2SO4=Na2SO4 + H2O +CO2↑;通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》:如图所示。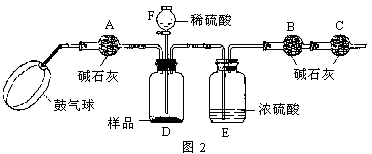
《实验步骤》:①如图连接装置(除B、C外)并加入所需药品。②称量并记录B的质量(m1) (称量时注意封闭B的两端) 。③按动鼓气球,持续约1分钟。④连接上B、C。⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。⑥按动鼓气球,持续约1分钟。⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)⑧计算。请回答:
(1)已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是 ,干燥管C的作用是 ,E装置的作用是 。步骤③中鼓气的目的是 ;步骤⑥中鼓气的目的是 ;本实验能否同时省略③、⑥两个步骤? ,原因是 。
(2)若所取样品的质量为5g,为确保实验顺利进行,分液漏斗F中至少要盛放10%的稀硫酸(密度为1.07g/mL) /mL,若m1为51.20 g ,m2为53.18g ,样品中碳酸钠的质量分数为 。
查看答案和解析>>
科目: 来源:2012届广西省贵港市初中毕业班第一次教学质量监测化学试卷(带解析) 题型:计算题
为测定黄铜(由锌、铜形成的合金)样品中铜的质量分数,往样品中加入稀硫酸充分反应,所加稀硫酸与剩余固体质量关系如右图所示。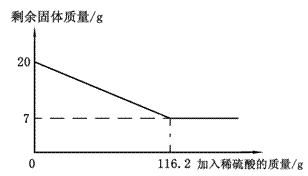
(1)样品中铜的质量分数。
(2)恰好完全反应时,所得溶液中溶质的质量分数。
查看答案和解析>>
科目: 来源:2012届四川省届南充市阆中中学九年级下学期第一次月度检测化学试卷(带解析) 题型:计算题
(6分)小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%。小明想:这瓶白醋中醋酸的含量是否与标签的标注相符?请你用有关酸碱的知识,定量测定白醋中醋酸的含量。
《实验原理》
⑴用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:
CH3COOH + NaOH = CH3COONa + H2O
⑵在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05 ml,对测定结果的影响很小,可忽略不计。
《实验步骤》
⑴用 取12.0 mL白醋(密度近似为1.0g/ ml),倒入烧杯中,加入20 ml蒸馏水稀释,再滴入几滴酚酞试液。
⑵量取45.0 ml溶质质量分数为1.0%的氢氧化钠溶液(密度近似为1.0 g/ ml),用胶头滴管取该氢氧化钠溶液,逐滴地滴加到稀释后的白醋中,同时不断地搅拌烧杯中的溶液。滴至恰好完全反应,剩余氢氧化钠溶液5.0 ml。
《交流反思》⑴在实验步骤①中,加适量水稀释白醋,对实验结果有无影响?为什么?
⑵在实验步骤②中,小明如何确定醋酸和氢氧化钠已完全中和?
《数据处理》根据实验数据,通过计算判断白醋中醋酸的含量是否与标签的标注相符?(3分)
查看答案和解析>>
科目: 来源:2012届江苏省江都市中考二模化学试卷 题型:计算题
某校研究性学习小组进行了一个有趣的实验探究:
《提出问题》实验室有一瓶久置的NaOH,变质程度怎样?
《设计方案》先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3
的质量,从而进一步确定样品中NaOH的质量分数。
《进行实验》实验测得加入稀盐酸的质量与产生CO2气体的质量关系如下图所示。
《数据处理》写出以下计算过程: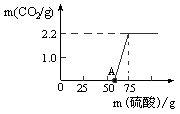
(1)该样品中Na2CO3的质量为多少?(2分)
(2)该样品中NaOH的质量分数为多少?(2分)
《反思与交流》①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入强酸,首先反应的物质是 ;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗强酸的量 。
查看答案和解析>>
科目: 来源:2012届黑龙江省哈尔滨市松北区中考调研测试一化学试卷 题型:计算题
(5分)某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数。取20g石灰石样品(假设杂质既不溶于水,也不与其他物质反应),向其中加入100g溶质质量分数为10.95%的稀盐酸,恰好完全反应.请回答下列问题。
(1)欲配制100g上述实验所用的稀盐酸,需要36.5%的浓盐酸质量为________________
(2)写出反应的化学方程式 ________________
(3)列出求解该样品申参加反应的碳酸钙质量(x)的比例式 ________
(4) 该样品中碳酸钙的质量分数为________
(5)向反应后的固液混合物中加入l13.6g水.充分搅拌后过滤,得到只含一种溶质的不饱和溶液,则所得不饱和溶液中溶质的质量分数为________________
查看答案和解析>>
科目: 来源:2012届四川省宜宾市中考模拟化学试卷 题型:计算题
(3分)某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12g纯碱样品放入烧杯中,称得烧杯及纯碱样品的总质量为158g,再把100g稀盐酸平均分成四份,依次加入到样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
查看答案和解析>>
科目: 来源:2012届江苏省泰兴市九年级3月月考化学试卷 题型:计算题
家庭食用面碱(主要成分为Na2CO3)中往往混有少量NaCl。李童同学为测定食用面碱中碳酸钠的含量,设计并进行了以下实验:
①称取面碱样品3.4g于烧杯中,加入20mL水,搅拌至样品全部溶解;
②向其中加入足量的CaCl2溶液,至不再生成沉淀为止;
③过滤并将所得沉淀干燥后,称得质量为3.0g(不考虑操作中的质量损失)。
请计算:食用面碱中Na2CO3的质量分数是多少?(精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com