
科目: 来源:2012届浙江省台州市八校九年级上学期期中联考化学试卷(带解析) 题型:计算题
现代生活中,人们越来越注意微量元素的摄入。血红蛋白中的铁是人体内氧的输送者,缺铁易患贫血。
(1)一种添加了营养剂的“铁强化”酱油已经面市。根据卫生部铁强化剂添加标准,每100mL酱油中铁营养剂添加量是200mg,该营养铁元素质量分数为12.5%。根据实验测得,酱油中铁只有10%能被人体吸收,以某人一天使用16mL该酱油计算,他一天从酱油中吸收的铁元素是多少毫克?
(2)某贫血患者除正常饮食吸收铁元素外,还需服用含铁元素的某种药物。若治疗一个疗程需补充1.12g铁元素,则服用药物中的铁元素相当于需要硫酸亚铁晶体(FeSO4?7H2O)多少克?
查看答案和解析>>
科目: 来源:2012届山东省济南市天桥区一模化学试卷(带解析) 题型:计算题
(6分)现有一瓶久置的标有质量分数为10%的NaOH溶液样品,为探究其变质(NaOH易和空气中的CO2反应生成Na2CO3)的相关问题,利用∪形管设计如下图所示的装置进行实验。
(1)如图46-1所示,若此溶液变质,分别在∪形管的两端滴入HCl溶液和澄清的石灰水时,观察到的现象:a端 ,b端 。
(2)如图46-2所示,取此NaOH样品溶液20g于∪形管中,并在其中加入适量的酚酞试液,通过分液漏斗向∪形管中滴入HCl溶液,当滴入20gHCl溶液时,恰好反应完全。
①滴入稀盐酸过程中,∪形管中的溶液颜色变化为 ;
②恰好完全反应时,生成气体0.22g,试通过计算得出20gNaOH样品溶液中所含Na2CO3的质量。
查看答案和解析>>
科目: 来源:2012届江苏省南京学大教育专修学校九年级2月测试化学试卷(带解析) 题型:计算题
某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应)。请计算:
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 20 | 11 |
| 第2次 | 20 | 6 |
| 第3次 | 20 | 2.8 |
| 第4次 | 20 | n |
查看答案和解析>>
科目: 来源:2012届江苏省南京学大教育专修学校九年级2月测试化学试卷(带解析) 题型:计算题
某样品为铜和氧化铜的混合物,为测定该样品中氧化铜的含量,取用20g此样品,分四次向其中加入稀盐酸与之充分反应。每次所用盐酸的体积与反应后剩余固体的质量见下表:
| 第次 | 加入稀盐酸的体积/mL | 剩余固体的质量/g |
| 1 | 40 | 16 |
| 2 | 40 | 12 |
| 3 | 40 | 8 |
| 4 | 40 | 8 |
查看答案和解析>>
科目: 来源:2011-2012学年度江西省桑海中学初三年级第二次联考化学试卷(带解析) 题型:计算题
现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液。为了测定碱性调味液中碳酸钠的质量分数,某同学进行了如下实验:取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某浓度的稀硫酸中,测得三组实验数据见下表(气体的溶解忽略不计):
根据实验及有关数据进行计算:
(1)100g碱性调味液与稀硫酸完全反应生成气体的质量为 g。
(2)碱性调味液中碳酸钠的质量分数为多少?
(3)100g碱性调味液与该稀硫酸反应后溶液pH=7时,消耗稀硫酸的质量为多少克?
查看答案和解析>>
科目: 来源:2012届重庆市重庆一中九年级上学期期末考试化学试卷(带解析) 题型:计算题
(6分) 兴趣小组同学为测定汉白玉中碳酸钙的质量分数,称取11.1g研碎的汉白玉粉末进行四次高温加热、冷却、称量剩余固体的重复操作(已知:杂质中不含钙元素,且不参加反应)。记录数据如下:
| 操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固体质量(g) | 8.5 | 6.9 | 6.7 | 6.7 |
查看答案和解析>>
科目: 来源:2012届江苏省东台市新曹农场中学初三年级阶段形成性测试化学试卷(带解析) 题型:计算题
(1)(8分)小丽在购买的袋装薯片中发现有一个小袋,上面标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色的,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,小丽打算进行实验探究,请你一同参与。
《实验目的》证实灰白色粉末中含有CaCO3和Fe。
《查阅资料》①氢气具有还原性,能夺取某些金属氧化物中的氧,使金属还原,
②白色的无水硫酸铜遇水变成蓝色。
《实验设计》装置如下图所示:
《实验预测与分析》
①若要证实样品中含有CaCO3,B中观察到的实验现象是_____________________,B中发生反应的化学方程式为_____________________。
②若要证实样品中含有Fe,D中应观察到的实验现象是________________________,E中应观察到的实验现象是________________________。
③看了小丽的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式__________________。
④小丽认为棕红色粉末Fe2O3也能与盐酸反应,请你写出反应的化学方程式___________________________。
(2)(5分)黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。为测定某黄铜中铜的质量分数,现取20g该样品粉碎,加入到100g稀硫酸中,恰好完全反应,反应后测得烧杯中剩余物的总质量为119.6克。
①反应生成氢气的质量是__________________,
②黄铜样品中铜的质量分数是_______________,
③计算稀硫酸中溶质的质量分数。
查看答案和解析>>
科目: 来源:2011-2012学年福建省仙游县九年级下册第一次月考化学试卷(带解析) 题型:计算题
12g镁与100g稀硫酸溶液恰好完全反应(化学方程式:Mg+H2SO4= MgSO4+ H2↑),请计算:
(1)生成氢气的质量;
(2)该硫酸溶液中溶质的质量分数。
查看答案和解析>>
科目: 来源:2012届江苏省镇江市实验初中九年级第二学期第一次素质调研化学试卷(带解析) 题型:计算题
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4 = Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》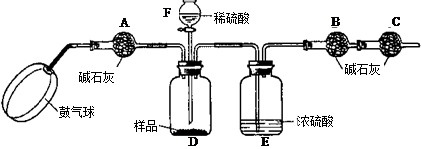
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
查看答案和解析>>
科目: 来源:2011-2012学年天津市宝坻八中九年级结课考试化学试卷(带解析) 题型:计算题
(7)向25.8g含有少量氯化钠杂质的碳酸钠白色固体中,慢慢加入10%的稀盐酸到恰好不在产生气体为止,共收集到气体8.8g。白色固体中碳酸钠的质量是多少?所得溶液中氯化钠的质量分数是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com