
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:填空题
环境的问题备受关注。
(1)化石燃料煤、石油和 的燃烧,造成了温室效应,控制二氧化碳排放,
充分利用和开发太阳能、核能及 (只填一种)等新能源。
(2)今年我国有些地区曾出现过严重的雾霾天气,造成的雾霾天气的原因是空气中增加
大量的 (填字母序号)
A.二氧化碳 B.一氧化碳 C.二氧化硫 D.可吸入颗粒物
(3)下列治理空气污染的方法和做法中可行的是(填序号)。
A.实施绿化工程,防治扬尘污染 B.禁止使用煤、石油、天然气等化石燃料
C.使用清洁能源 D.分类回收垃圾,并露天焚烧
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:探究题
在学习过程中,可以判断反应发生的方法有多种。
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
|
加入NaOH溶液的体积/mL |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
|
烧杯中溶液的pH |
1.1 |
1.2 |
1.4 |
1.6 |
2.0 |
7.0 |
11.0 |
12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
(2)在图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应。

(3)不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该合理的物质是 。
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:填空题
人类的生产生活离不开金属。
(1)在地壳里含量最多的金属元素是 。
(2)我国是世界上最早使用湿法炼铜的国家,其反应原理是 。(用
化学方程式表示)。下列铜制品的用途中,利用金属导电性的是 (填字母)。

A.铜火锅 B.铜导线 C.铜钟 D.铜钱
(3)铁在同时有水和 的条件下易生锈;金属铜长期暴
露在空气中也容易被锈蚀的,铜锈的化学式为Cu2(OH)2CO3,其
生锈的条件与铁有相似之处,另外,还可能与空气中的 有关。
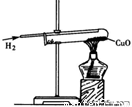
(4)下图是实验室用氢气还原氧化铜实验的示意图。实验结束后,某同学发现试管里红色的物质又变成黑色,原因是 。
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:填空题
下图表示的是在高温条件下,A、B两种物质发生化学反应生成C和D的微观示意图。

请回答下列问题。
(1)写出该反应的化学方程式 。
(2)若反应后生成D的质量为3g,则生成C的质量为 。
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:推断题
有一固体粉末,可能含有氯化钠、碳酸钠、硫酸钠和硝酸钙,进行如图实验,由图可知,固体粉末中一定含有 ,一定不含有 。
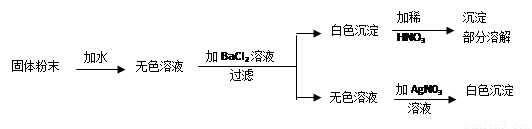
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:填空题
某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如下:①按图连接装置;②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为m1克;③准确称得m2克的纯碱样品放入容器b中;④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为m3克;⑥根据测得的数据分析计算碳酸钠的质量分数。试回答:

(1)在步骤①连接装置后还应 ;
(2)装置A中试剂可选用 ;
(3)写出装置B中的反应方程式 ;
(4)若没有C装置,则会导致测定结果 (填“偏大”或“偏小”);
(5)步骤⑤的目的是__ __;
(6)E装置的作用是__ __。
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:探究题
为检测某化工厂排放的废液中是否含有SO42-,同学们设计了如下方案,并进行了实验。
|
方案 |
步骤 |
现象 |
结论 |
|
Ⅰ |
①取样品,滴加BaCl2溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有SO42﹣ |
|
Ⅱ |
①取样品,滴加过量_____________ ②在步骤①的溶液中滴加BaCl2溶液 |
①无明显现象 ②有白色沉淀产生 |
废液中含有SO42- |
|
Ⅲ |
①取样品,滴加Ba(NO3)2溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 |
①有白色沉淀产生 ②无明显现象
|
废液中含有SO42- |
(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是 。21世纪教育网
(2)方案Ⅰ和Ⅲ中,结论不成立的方案是 ,理由是 。
(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除 的干扰。
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:探究题
小红为大家做了一个“燃纸成铁”的趣味实验。将一张滤纸(组成元素为C、H、O)用FeCl3 浓溶液润湿,在酒精灯上烘干后点燃,滤纸变黑、红热,最终生成黑褐色物质。小红告诉大家:黑褐色物质中含有铁单质。
【提出问题】黑褐色物质中真的含有铁单质吗?
【探究过程】
(1)小红先从反应物组成分析,因为 所以反应后可能生成铁单质。
(2)为获得实验证据,小红做了实验1。
实验1:将黑褐色物质放入稀盐酸中,发现有连续微小气泡产生。若黑褐色物质中
含有铁单质,则反应的化学方程式为 。
(3)小明提出疑问:实验1中产生的气泡也可能是滤纸碳化后吸附的空气。为此,小红又做了实验2: 观察到有微小气泡产生但很快停止。
证明实验1中的连续气泡确实是由铁单质与稀盐酸反应产生的。
(4)为进一步证明黑褐色物质中有铁单质,小红又做了实验3。
实验3:将黑褐色物质放入 溶液中,观察到红色物质生成。
【得出结论】通过以上实验探究,证明黑褐色物质中确实含有铁单质。
(5)【实验反思】小红所做实验1和实验2是运用了 实验,使结论更有说服力。
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:计算题
某硫酸厂废水中含有少量硫酸,为达标排放,技术员小张对废水中硫酸的含量进行检测.
(1)配制溶液: 欲配制溶质质量分数为4%的NaOH溶液100g,需要NaOH固体 g,水 ml(水的密度为1g/cm3);
(2)检测分析: 取废水样品98g,向其中逐滴加入NaOH溶液至恰好完全反应时,消耗4%的NaOH溶液20g。(假设废水中其它成分均不和NaOH反应;发生反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O); 试计算废水中硫酸的质量分数(写出计算过程).
查看答案和解析>>
科目: 来源:2013-2014学年浙江省九年级上学期期中考试化学试卷(解析版) 题型:计算题
现有Cu与另一种金属(可能是Mg、Fe、Zn中的一种)形成的粉末。现欲测定其组成,进行如下实验:取该粉末16g放入烧杯,将溶质质量分数为14%的稀硫酸280.0g分4次加入该烧杯中,充分反应后,测得剩余的固体质量数据记录如下:
|
实验次数 |
1 |
2 |
3 |
4 |
|
加入稀硫酸质量/g |
70.0 |
70.0 |
70.0 |
70.0 |
|
剩余固体质量/g |
13.6 |
11.2 |
8.8 |
8.4 |
计算(要求写出计算过程):
(1)该粉末中Cu的质量分数。
(2)该粉末中另一种金属为何种金属。
(3)第3次加入稀硫酸充分反应后,所得溶液中溶质的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com