
| 13 |
| 2 |
| 13 |
| 2 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 0.025 |
| 1 |
| 4 |
| 1 |
| 0.05 |


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
| 选项 | 需除杂的物质 | 试剂 | 操作 |
| A | NaCl(Na2CO3) | 稀盐酸 | 蒸发结晶 |
| B | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| C | Cl2(H2O) | 碱石灰 | 洗气 |
| D | CO2(CO) | -- | 点燃 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
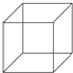 (1)键线式
(1)键线式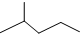 表示的分子式
表示的分子式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
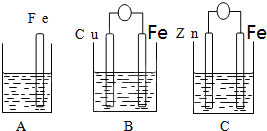
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com