
A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大。其中, 元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种, 其中一种是红棕色气体。
(1)M的基态原子价层电子排布式为_____,元素B、D、G的第一电离能由大到时小的顺序是_____ (用元素符号表示)。
(2)用价层电子对互斥理论预测,GD32-的立体构型是_____ (用文字表述)
(3)M与D形成的一种橙红色晶体晶胞结构如图所示,其化学式为_____ (用元素符号表示)。

(4)已知化合物EB结构与单晶硅相似,该物质可由E 的氯化物与NaB3在高温下反应制得,且生成单质B2,该反应化学方程式为_____,若有8.4gB2生成,则转移电子数为_____。
(14分)
(1)3d24s2(2分) N>O>S(2分)
(2)三角锥形(2分)
(3)TiO2(3分)
(4)AlCl3+3NaN3= 3NaCl+AlN+4N2↑(3分) 1.204×1023或0.2NA(2分)
【解析】
试题分析:A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大。其中元素M的基态3d轨道上有2个电子,价层电子排布式3d24s2,为钪元素;A的基态原子L层电子数是K层电子数的2倍,元素A为碳元素,E的简单离子在同周期元素的简单离子中半径最小,元素E为铝;B与D形成的化合物有多种, 其中一种是红棕色气体,很显然元素B为氮元素,D为氧元素。D、G同主族,G为硫元素;
考点:考查元素的核外电子排布式、元素的杂化类型,元素原子半径比较。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
| A | ||||||||||||||||||
| M | B | D | ||||||||||||||||
| G | H | Q | R | |||||||||||||||
| E | ||||||||||||||||||


查看答案和解析>>
科目:高中化学 来源: 题型:
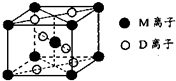 (2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.
(2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.查看答案和解析>>
科目:高中化学 来源: 题型:











| 燃烧有机物的质量 | 实验方法 | 实验前后①-④装置质量 | |||
| 实验前 | 实验后 | ||||
| 甲组 | 5.4g | A | ①150g | ①153.6g | |
| ②150g | ②165.4g | ||||
| 乙组 | 5.4g | B | ③150g | ③166.0g | |
| ④150g | ④154.2g | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
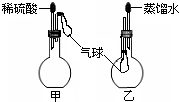 A、B、D、E、G为短周期元素,其原子序数依次增大.A元素在周期表中原子半径最小,B元素的最高正化合价和最低负化合价的绝对值相等,E元素的原子最外层电子数是次外层的3倍.E和G可形成离子化合物GE.
A、B、D、E、G为短周期元素,其原子序数依次增大.A元素在周期表中原子半径最小,B元素的最高正化合价和最低负化合价的绝对值相等,E元素的原子最外层电子数是次外层的3倍.E和G可形成离子化合物GE.
| ||
| ||
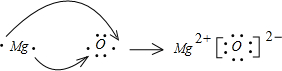
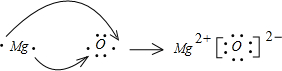
查看答案和解析>>
科目:高中化学 来源: 题型:


| ||
| ||
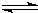 NH4++OH-
NH4++OH-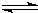 NH4++OH-
NH4++OH-查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com