
科目: 来源: 题型:
在恒容密闭容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应:CO2(g)+CH4(g)2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示,下列有关说法一定正确的是( )
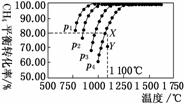
A.上述反应的ΔH>0
B.压强p1>p2>p3>p4
C.1 100 ℃该反应的平衡常数为64
D.压强为p4时,在Y点:v(正)<v(逆)
查看答案和解析>>
科目: 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0 ~6.0之间,通过电解生成Fe(OH)3 沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计如图所示装置示意图。
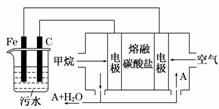
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的________。
A.BaSO4 B.CH3CH2OH
C.Na2SO4 D.NaOH
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:
Ⅰ.______________;Ⅱ.______________。
(3)电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH)3沉淀的离子方程式是________________________________________________________________________。
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料作电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是______________________。
查看答案和解析>>
科目: 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
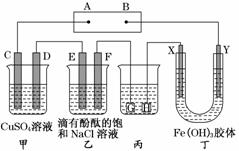
请回答:
(1)B极是电源的______________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明_____________________________,
在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________。
(3)现用丙装置给铜件镀银,则H应是______________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时 (此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
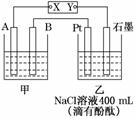
如图为相互串联的甲乙两个电解池,X、Y为直流电源的两个电极。电解过程中,发现石墨电极附近先变红。请回答:
(1)电源X极为________极(填“正”或“负”),乙池中Pt电极上的电极反应式为______________________________________。
(2)甲池若为电解精炼铜的装置,其阴极增重12.8 g,则乙池中阴极上放出的气体在标准状况下的体积为________,电路中通过的电子为________ mol。
(3)在(2)的情况下,若乙池剩余溶液的体积仍为400 mL,则电解后所得溶液c(OH-)=________。
查看答案和解析>>
科目: 来源: 题型:
按如图所示装置进行实验,并回答下列问题:
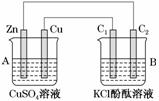 (1)判断装置的名称:A池为________,B池为________________。
(1)判断装置的名称:A池为________,B池为________________。
(2)锌极为________极,电极反应式为__________________;
铜极为________极,电极反应式为________________________________________
________________________________________________________________________;
石墨棒C1为____极,电极反应式为______________________________________
________________________________________________________________________;
石墨棒C2附近发生的实验现象为________________________________________
________________________________________________________________________。
(3)当C2极析出224 mL气体(标准状况)时,锌的质量________(填“增加”或“减少”)________g,CuSO4溶液的质量________(填“增加”或“减少”)________g。
查看答案和解析>>
科目: 来源: 题型:
假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。下列说法错误的是( )
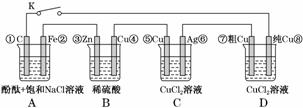
A.当K闭合时,A装置发生吸氧腐蚀,在电路中作电源
B.当K断开时,B装置锌片溶解,有氢气产生
C.当K闭合后,整个电路中电子的流动方向为①→⑧;⑦→⑥;⑤→④;③→②
D.当K闭合后,A、B装置中pH变大,C、D装置中pH不变
查看答案和解析>>
科目: 来源: 题型:
某同学按下图所示的装置进行实验。A、B为两种常见金属,它们的硫酸盐可溶于水,当K闭合时,SO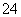 从右向左通过交换膜移向A极。下列分析正确的是( )
从右向左通过交换膜移向A极。下列分析正确的是( )
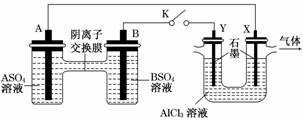
A.溶液中c(A2+)减小
B.B极的电极反应:B-2e-===B2+
C.Y电极上有H2产生,发生还原反应
D.反应初期,X电极周围出现白色胶状沉淀
查看答案和解析>>
科目: 来源: 题型:
用铅蓄电池电解AgNO3、Na2SO3的溶液,a、b、c、d电极材料均为石墨。已知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l),通电时a电极质量增加,下列说法正确的是( )
2PbSO4(s)+2H2O(l),通电时a电极质量增加,下列说法正确的是( )
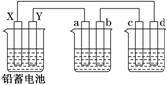
A.电路中通过1 mol电子时, Y电极质量增加48 g
B.放电时铅蓄电池负极的电极反应式为:
PbO2(s)+4H+(aq)+SO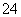 (aq)+2e-===PbSO4(s)+2H2O(l)
(aq)+2e-===PbSO4(s)+2H2O(l)
C.c、d电极产生气体的物质的量之比为1∶2
D.X极为负极
查看答案和解析>>
科目: 来源: 题型:
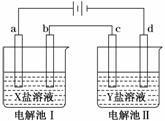
下图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是( )
| 选项 | X | Y |
| A | MgSO4 | CuSO4 |
| B | AgNO3 | Pb(NO3)2 |
| C | FeSO4 | Al2(SO4)3 |
| D | CuSO4 | AgNO3 |
查看答案和解析>>
科目: 来源: 题型:
铅蓄电池的工作原理为: Pb+PbO2+2H2SO4===2PbSO4+2H2O。研读下图,下列判断不正确的是( )
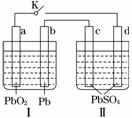
A. K闭合时,d电极反应式:PbSO4+2H2O-2e-===PbO2+4H++SO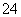
B. 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C. K闭合时,Ⅱ中SO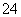 向c电极迁移
向c电极迁移
D. K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com