
科目: 来源: 题型:
.现有A、B、C、D四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:A < C < B < D Ⅱ.原子的最外层电子数:A + C = B + D = 8
Ⅲ.原子的核外电子层数:B = C = 2A Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)由A、B两种元素组成的常见气体,其电子式为 ;只有A和B两种元素组成的属于离子晶体的化合物可能为 (用化学式表示)。
(2)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为 。
(3)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式 。
(4)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,则0.1 mol·L-1 该盐溶液中浓度最大的离子为 (写离子符号);写出检验该盐中所含阳离子的实验方法 。
查看答案和解析>>
科目: 来源: 题型:
原子序数依次递增的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期。已知
X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼
铁;Z与X同主族,其单质在同周期元素形成的单质中熔点最高;W原子M能层为全充满
状态,且核外的未成对电子只有一个。回答下列问题:
(1)从电负性角度分析,X,Y,Z三种元素的非金属活泼性由强到弱的顺序为 。
(2)X、Y分别与H形成的化学键的极性关系为X-H Y-H(填“<”、“>”或“=”)。
(3)+l价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二
电离能I2,依次还有I3、I4、I5…,推测Z元素的电离能突增应出现在第____电离能。
(4)X的氢化物中X原子的杂化方式为sp2,则相对分子质量最小的分子式为____,
(5)W的价电子排布图为 ;下图____表示的是W晶体中微粒的堆积方式(填甲、乙或丙);若W晶体中一个晶胞的边长为a cm,则W晶体的密度为____(写出含a的表达式,用NA表示阿伏伽德罗常数)。

查看答案和解析>>
科目: 来源: 题型:
下列有关用途的说法中,错误的是:
A.液态钠可用作核反应堆的传热介质
B.在过渡元素中找寻半导体材料
C.考古时利用l4C测定一些文物的年代
D.SiO2是制造水泥、人造宝石、单晶硅的原料
查看答案和解析>>
科目: 来源: 题型:
下列说法合理的是
A.若X+ 和Y2 - 的核外电子层结构相同,则原子序数:X>Y
B.由水溶液的酸性:HCI>H2S,可推断出元素的非金属性:CI>S
C.邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键
D.H—F、H—O、H—N三种共价键的极性逐渐增强
查看答案和解析>>
科目: 来源: 题型:
下列各组顺序排列正确的是
A.密度:Na > K > Li B.热稳定性:HCl > H2S > H2O
C.酸性:H2CO3 < H2SiO3 < HNO3 D.离子半径:F -> A13+ > CI –
查看答案和解析>>
科目: 来源: 题型:
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的电子排布式为
(2)钛能与B、C、 N、 O等非金属元素形成稳定的化合物。电负性:C (填“>”或“<”下同)B;第一电离能: N O。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3) 。 FeTiO3与80%的硫酸反应可 生成TiOSO4。SO42-的空间构型为 形,其中硫原子采用 杂化.
(4)磷酸钛〔Ti3 (PO4 )4]锂离子电池能量密度大、安全性高。Ti3 (PO4 )4可由TiOSO4与
 H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
则三分子H3PO4脱去两分子H2O生成三磷酸,其结构式为 ,四分子H3PO4 脱去四分子H2O生成的四偏磷酸属于 元酸。
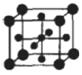
(5)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图所示(Ti4+位于立方体的顶点)。该晶体中,Ti4+和周围 个O2-相紧邻.
(6)Fe能形成多种氧化物,其中FeO晶胞结构为NaCI型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1)中,若测得某FexO晶体密度为5.71 g·cm-3,晶胞边长为4.28X10-10 m,则FexO中x=_。
查看答案和解析>>
科目: 来源: 题型:
设NA 为阿伏加德罗常数的值。下列说法正确的是 ( )
A.标准状况下,2.24 L 水中所含的电子数为NA
B.常温常压下,16 g O3所含的电子数为8NA
C.0.1 mol Na2O2 晶体中所含的离子数为0.4NA
D.1 mol Fe在氧气中充分燃烧失去的电子数为3NA
查看答案和解析>>
科目: 来源: 题型:
)合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为: Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac 。完成下列填空:
[Cu(NH3)3CO]Ac 。完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是 。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式_____________________
(3)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为__________________。通过比较_____________________________可判断氮、磷两种非金属元素的非金属性强弱。
(4)已知CS2与CO2分子结构相似,CS2的电子式是_________________。CS2熔点高于CO2,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
.X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见气体甲。X、Y、Z 3种元素形成化合物乙。下列说法不正确的是 ( )
A.原子半径:W>Y>Z>M>X B.化合物乙中一定只有共价键
C.由W元素形成的单质以及W与Z两元素形成的化合物都是原子晶体
D.X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM
查看答案和解析>>
科目: 来源: 题型:
A—I为原子序数递增的前4周期的元素,已知A原子的最外层电子是次外层电子数的2倍,D为周期表中电负性最大的元素,F与C位于同一主族,E与G在周期表的位置是上下相连,两元素所在主族中所有元素都是金属,H为应用最广泛的金属;I处于周期表中的第二副族。请回答下列问题:(以下问题中的所有原子都必须在上述元素中寻找)
(1)B单质分子中σ与π键数目比为 B、C、D第一电离能由小到大的顺序为 (填写元素符号)
 (2)H元素原子的价层电子排布式为 ,H3+离子可以与上述元素中的三种形成的某阴离子生成血红色络合物;该阴离子又与A—I元素中的某些原子形成的分子互为等电子体,这种分子的化学式为 (写一种即可),该阴离子空间构型为 。
(2)H元素原子的价层电子排布式为 ,H3+离子可以与上述元素中的三种形成的某阴离子生成血红色络合物;该阴离子又与A—I元素中的某些原子形成的分子互为等电子体,这种分子的化学式为 (写一种即可),该阴离子空间构型为 。
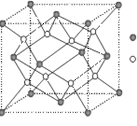
(3)D与G可以形成右图的晶胞,则黑点表示的是 元素(填写元素符号),该元素原子在该晶胞中的配位数为
(4)若将上述晶胞圆圈对应的原子所在上下两层平面原子,按两条相互垂直的对角线上各去掉该原子2个(共去掉4个),并将小点和圆圈对应的元素更改为另外两种元素,则这个晶胞化学式为 ,若再将留下的所有原子换成另外一种新元素的原子,则成为另外一种晶胞,该晶胞中成键原子键角为 。
(5)已知,F单质晶体的原子堆积为ABAB型,那么,该晶体的空间利用率为 如果F单质的摩尔质量为M,晶胞棱长为a,晶胞高度为c则,该晶体密度表达式为 。(阿伏加德罗常数用NA表示,不化简)如果F的原子半径为R,用R表示的晶胞高度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com