
科目: 来源: 题型:
向Fe2O3、CuO、Fe、Cu的混和粉末中加入过量的稀盐酸,充分反应后,仍有红色粉末存在,则关于溶液中阳离子的判断正确的是()
A. 只有Fe2+和Cu2+
B. 一定有Fe2+、Cu2+,可能有Fe3+
C. 一定有Fe2+,可能有Cu2+
D. 只有Fe2+
查看答案和解析>>
科目: 来源: 题型:
向一定量的FeO、Fe、Fe2O3的混合物中加入100ml1mol/L的盐酸,恰好使混合物完全溶解,放出224ml标况下的气体,在所得溶液中滴入硫氰化钾溶液无血红色出现(即无3价铁).若用足量CO在高温下还原同质量的此混合物,能得到铁的质量是()
A. 11.2g B. 5.6g C. 2.8g D. 无法计算
查看答案和解析>>
科目: 来源: 题型:
同温同压下,在3支体积不同的试管中分别充满等体积混合的2种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2.现将3支试管均倒置于水槽中,充分反应后,试管中溶质的物质的量浓度分别为c1、c2、c3(假设溶质全在试管中),则下列关系正确的是()
A. c1>c2>c3 B. c1>c3>c2 C. c1=c3>c2 D. c1=c2>c3
查看答案和解析>>
科目: 来源: 题型:
如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是()
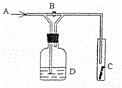
A. 浓H2SO4 B. 饱和Na2CO3溶液
C. 浓NaOH溶液 D. 饱和NaCl溶液
查看答案和解析>>
科目: 来源: 题型:
下列溶液中:①石灰水 ②Na2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液,不能区别SO2和CO2气体的是()
A. ②④⑤ B. ①② C. ①②⑤ D. 只有①
查看答案和解析>>
科目: 来源: 题型:
对某酸性溶液(可能含有Br﹣,SO42﹣,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸.
对于下列物质不能确认其在原溶液中是否存在的是()
A. Br﹣ B. SO42﹣ C. H2SO3 D. NH4+
查看答案和解析>>
科目: 来源: 题型:
下列推断正确的是()
A. SiO2是酸性氧化物,能与NaOH溶液反应
B. Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C. CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D. 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
查看答案和解析>>
科目: 来源: 题型:
关于合金的叙述:①合金中至少含两种金属;②合金中的元素以化合物的形式存在;③合金中一定含金属;④合金一定是混合物.其中正确的是()
A. ①②③④ B. ①③④ C. ②③④ D. ③④
查看答案和解析>>
科目: 来源: 题型:
化学反应原理在生产、生活、国防上有重要的应用.例如:
联氨(N2H4)及其衍生物是一类重要的火箭燃料.N2H4与N2O4反应能放出大量的热.
①已知:2NO2(g)⇌N2O4(g)△H=﹣57.20kJ•mol﹣1.
一定温度下,在密闭容器中反应2NO2(g)⇌N2O4(g)达到平衡.
其他条件不变时,下列措施能提高NO2转化率的是 (填字母).
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
②下表为反应2NO2(g)⇌N2O4(g)在17℃、1.01×105Pa下的部分实验数据:
| 时间/s | 0 | 80 | 160 | 240 | 320 |
| c(NO2)/mol•L﹣1 | 0.0540 | 0.0420 | 0.0340 | 0.0300 | 0.0300 |
| c(N2O4)/mol•L﹣1 | 0 | 0.0060 | 0.0100 | 0.0120 | 0.0120 |
该温度下反应N2O4(g)⇌2NO2(g)的平衡常数K的值为 .
(写出计算过程)
③25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.
则该反应的热化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和另一种常见气体.进一步研究NH3生成量与温度的关系(其它条件均相同),部分实验数据见下表:
| T/K | 303 | 313 | 323 |
| 平衡时NH3的生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 |
回答下列问题:
(1)写出该反应的化学方程式
(2)该反应的焓变△H 0(填“>”、“<”或“=”)
(3)请在答题纸的坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注.
(4)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议: .
(5)已知:
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol
H2(g)+Cl2(g)═2HCl(g)△H=﹣184.6kJ/mol
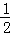 N2(g)+2H2(g)+
N2(g)+2H2(g)+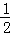 Cl2(g)═NH4Cl(s)△H=﹣313.6kJ/mol
Cl2(g)═NH4Cl(s)△H=﹣313.6kJ/mol
计算NH3(g)+HCl(g)═NH4Cl(s)的反应焓变:△H= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com