
科目: 来源: 题型:
设阿伏伽德罗常数的数值为NA,下列说法正确的是()
A. 1.8g NH4+含有的电子数为NA
B. 1mol Cl2与足量Fe反应,转移的电子数为3NA
C. 46g的NO2与46g的N2O4含有的原子数不同
D. 标准状况下11.2L苯完全燃烧产生二氧化碳分子数为3NA
查看答案和解析>>
科目: 来源: 题型:
某溶液中含有S2﹣、HCO3﹣、CO32﹣、CH3COO﹣4种阴离子.若向其中加入足量Na2O2后,溶液中离子数目基本保持不变的是()
A. S2﹣ B. HCO3﹣ C. CO32﹣ D. CH3COO﹣
查看答案和解析>>
科目: 来源: 题型:
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是()
①它们所含的分子数目之比为1:1
②它们所含的O原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们的质量之比为7:11.
A. 仅①和④ B. 仅②和③ C. 仅④和⑤ D. ①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
分类是化学学习和研究中的常有用手段,下列分类依据和结论都正确的是()
A. 浓HCl、浓H2SO4、浓HNO3均具有氧化性,都属氧化性酸
B. Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质
C. NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物
D. 金刚石、二氧化硅、碳化硅晶体中的原子均能共价键结合,都属原子晶体
查看答案和解析>>
科目: 来源: 题型:
以下最接近阿伏伽德罗常数的是()
A. 2.0L 1.Omol•L﹣1 CH3COOH溶液中的H+离子数
B. 2.0L 1.0 mol•L﹣1CH3COONa溶液中的CH3COO﹣离子数
C. 1.0L 1.0 mol•L﹣1NaHCO3溶液中的HCO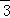 离子数
离子数
D. 1.0L 1.0 mol•L﹣1Na2CO3 溶液中的 C032﹣离子数
查看答案和解析>>
科目: 来源: 题型:
有机物D为烃类化合物,质谱图表明其相对分子质量为56,其相关反应如下图所示.其中A、C、E的结构中均含有2个﹣CH3,且它们的核磁共振氢谱中均出现3个峰.
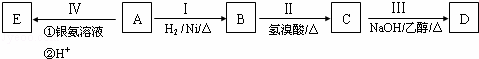
请回答:
(1)D的分子式为C4H8.
(2)写出下列反应的化学方程式:
Ⅱ:
Ⅲ:
(3)与D具有相同官能团的一种同分异构体存在顺反异构,请写出此反式结构的结构简式
(4)已知D经过反应可制得有机玻璃的单体F: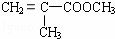 ,由单体F制有机玻璃的反应类型是 高聚物的结构简式是
,由单体F制有机玻璃的反应类型是 高聚物的结构简式是
(5)已知D经过反应可制得G: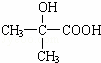 ,写出由G作为单体在一定条件下生成聚酯的化学方程式:
,写出由G作为单体在一定条件下生成聚酯的化学方程式:
查看答案和解析>>
科目: 来源: 题型:
电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置.
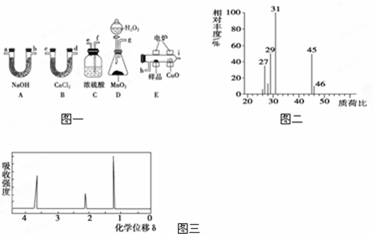
(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是g→f→e→h→i→c(或 .
(2)C装置中浓硫酸的作用是 .
(3)D装置中MnO2的作用是 .
(4)燃烧管中CuO的作用是 ;.
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为
(6)用质谱仪测定其相对分子质量,得如图一所示的质谱图,则该有机物的相对分子质量为 .
(7)能否根据A的实验式确定A的分子式能(填“能”或“不能”),若能,则A的分子式是 能,则此空不填).
(8)该物质的核磁共振氢谱如图二所示,则其结构简式为CH3CH2OH.
查看答案和解析>>
科目: 来源: 题型:
下列物质:①O2②三氯甲烷③CH3CH2CH2OH④O3⑤CHCl3 CH3OCH2CH3⑦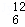 C ⑧CH3CH(OH)CH3⑨
C ⑧CH3CH(OH)CH3⑨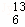 C ⑩CH3OH.
C ⑩CH3OH.
其中属于同系物的有 (填序号,下同),
互为同分异构体的有 ,
互为同素异形体的有 ,
属于同位素的有 ,
是同一种物质的有 .
查看答案和解析>>
科目: 来源: 题型:
开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池.
(1)已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ/mol
③H2O(g)=H2O(1)△H3=﹣44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: .
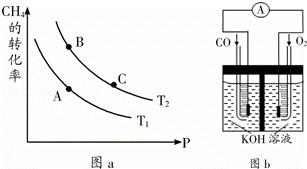
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H>0
①一定条件下CH4的平衡转化率与温度、压强的关系如图a.则Tl T2(填“<”、“>”、“=”,下同);A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为 .
②100℃时,将1mol CH4和2mol H2O通入容积为1L的定容密封容器中,发生反应,能说明该反应已经达到平衡状态的是 .
a.容器内气体密度恒定
b.单位时间内消耗0.1mol CH4同时生成0.3mol H2
c.容器的压强恒定
d.3v正(CH4)=v逆(H2)
如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=2.25.
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com