
科目: 来源:2016届云南师大附中高考适应性月考(四)理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述正确的是
A.红磷在氯气中反应,1mol红磷失去的电子数一定为5NA
B.标准状况下22.4L C3H8中含中子数为18NA
C.1L 1mol/L的葡萄糖溶液中,含有的分子数为NA个
D.常温下78 g过氧化钠和122 g水混合,所得溶液质量分数为40%
查看答案和解析>>
科目: 来源:2016届云南师大附中高考适应性月考(四)理综化学试卷(解析版) 题型:填空题
淡水是一种重要的自然资源,是人类赖以生存不可缺少的物质。按要求回答下列问题:
(1)水质优劣直接影响人体健康。天然水在净化处理过程中加入的混凝剂可以是___________(填一种物质的名称),其净水作用的原理是_________________________ ____。混凝剂难以清除溶解于水中的有机物、无机物、微生物,混凝剂沉淀后还需要_____________。
(2)硬水的软化指的是_________________________ ____________________________ ___。
(3)硬度为1°的水是指每升水含10mg CaO或与之相当的物质(如7.1mg MgO)。若某天然水中c(Ca2+)=1.2×10-3mol/L,c(Mg2+)=6×10-4mol/L,则此水的硬度为_____________。
(4)若(3)中的天然水还含有c(HCO3-)=8×10-4mol/L,现要软化10m3这种天然水,则需先加入Ca(OH)2____________g, 后加入Na2CO3___________g 。
(5)如图是电渗析法淡化海水的原理图,其中,电极A接直流电源的正极,电极B接直流电源的负极。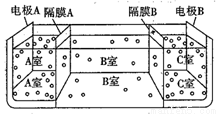
①隔膜A是_________(填“阴”或“阳”)离子交换膜。
②某种海水样品,经分析含有大量的Na+、Cl-,以及少量的K+、SO42-。若用上述装置对该海水进行淡化,当淡化工作完成后,A、B、C三室中所得溶液(或液体)的pH分别为pHa、pHb、pHc,则其大小顺序为________________________。
查看答案和解析>>
科目: 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
下列有关化学用语表达正确的是
A.质子数为92、中子数为146的U原子: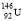
B. HClO的结构式:H-Cl-O
C. 35Cl-和37Cl-离子结构示意图均可以表示为: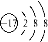
D.HF的电子式: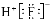
查看答案和解析>>
科目: 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
下列有关化工生产的叙述中,正确的是
A.工业上可用氯化钠制备化肥NH4Cl
B.氯碱工业中,电解槽的阳极区产生NaOH
C.在接触室被氧化成SO3,SO3在吸收塔内被水吸收制成浓硫酸
D.工业上用石英制太阳能电池,在高温下用铝热法炼铁制备钢材
查看答案和解析>>
科目: 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
亚氯酸钠是一种高效氧化剂漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示
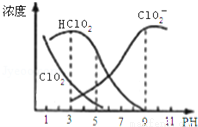
(Cl﹣没有画出).则下列分析正确的是
A.亚氯酸钠在酸性条件下较稳定
B.25℃时,HClO2的电离平衡常数的数值Ka=10﹣6
C.pH越大,该漂白剂的漂白性能越好
D.25℃,pH=3时,NaClO2溶液中:c(Na+)+(H+)=c(ClO2-)+c(OH-)
查看答案和解析>>
科目: 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
常见的无机酸25℃时在水溶液中的电离平衡常数如下表,下列选项正确的是
氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
K = 6.2×10-10 | Ka1= 4.2×10-7 | K=6.61×10-4 |
A.氟化钠溶液中通入CO2:2F-+H2O+CO2=2HF+CO32-
B.NaCN与HCN的混合溶液中:2c(Na+) = c(CN-)+ c(HCN)
C.0.2 mol•L-1 HCN溶液与0.1 mol•L-1NaOH溶液等体积混合后,溶液的pH>7
D.25℃时同浓度的NaCN和NaF溶液的pH值前者小于后者
查看答案和解析>>
科目: 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合
B.用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值
C.H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快
D.欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)分别为中和滴定实验和pH试纸
查看答案和解析>>
科目: 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:填空题
雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一。已知汽车尾气排放时容易发生以下反应:
①N2(g)+O2(g) 2NO(g)△H1=a kJ•mol﹣1
2NO(g)△H1=a kJ•mol﹣1
②2NO(g)+O2(g) 2NO2(g)△H2=b kJ•mol﹣1
2NO2(g)△H2=b kJ•mol﹣1
③CO(g)+1/2O2(g) CO2(g)△H3=c kJ•mol﹣1
CO2(g)△H3=c kJ•mol﹣1
④2CO(g)+2NO(g) N2(g)+2CO2(g)△H4
N2(g)+2CO2(g)△H4
请回答下列问题:
(1)根据反应①②③,确定反应④中△H4 = kJ•mol﹣1。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应①的Kp= (用表达式表示).
(3)下列情况能说明反应②已达平衡状态的是 (填编号).
A.单位时间内生成1mol NO2的同时消耗了lmol NO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,NO的体积分数保持不变
(4)探究反应④中NO的平衡转化率与压强、温度的关系,得到如图1所示的曲线.试分析实际化工生产中不采用高压的原因 。
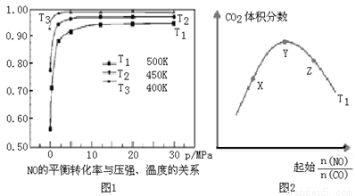
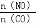 (5)探究反应④中平衡时CO2的体积分数与反应物中 的比值、温度的关系,得到如图2所示的曲线。
(5)探究反应④中平衡时CO2的体积分数与反应物中 的比值、温度的关系,得到如图2所示的曲线。
①在X、Y、Z三点中,CO的转化率从大到小的顺序是 。
②若保持其他条件不变,请在图2中,画出温度为T2(T2<T1)时的变化趋势曲线。
查看答案和解析>>
科目: 来源:2015-2016学年广东广州执信中学高二上期中理化学试卷(解析版) 题型:选择题
下列实验操作合理的是
A.用托盘天平称一定质量的NaOH固体,两端应同时放上一张滤纸再调平
B.用25 mL的碱式滴定管量取14.80 mL的NaOH溶液
C.25 mL的酸式滴定管装 0.1 mol/L的H2SO4溶液至0.00 刻度,则所盛溶液体积为25.00 mL
D.用量筒量取一定体积的溶液前,必须先用该溶液润洗
查看答案和解析>>
科目: 来源:2015-2016学年广东广州执信中学高二上期中理化学试卷(解析版) 题型:选择题
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni (s)+4CO (g)  Ni(CO)4 (g),已知该反应平衡常数与温度的关系如表:
Ni(CO)4 (g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是
A. 上述生成Ni(CO)4 (g)的反应为放热反应
B. 25℃时反应Ni(CO)4 (g)  Ni (s)+4CO (g)的平衡常数为2×10﹣5
Ni (s)+4CO (g)的平衡常数为2×10﹣5
C. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com