
科目: 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:推断题
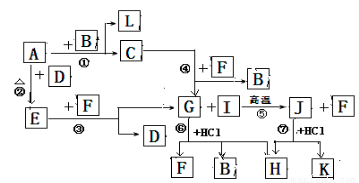
(6分)下图为由短周期元素形成的物质之间的转化关系,其中A、D、L为单质,其它为化合物。其中化合物I、J、K中含有两种相同的元素,G和I的反应⑤是一种重要化工生产中的主要反应之一。B常温下为液态化合物,F是中学化学中常见的气体,其固体易升华,可用于人工降雨。
试回答下列有关问题:
(1)以上7个化学反应属于氧化还原反应的是 (用编号①→⑦填写)
(2)G、J、H中含有的相同的元素是______________;
(3)J的水溶液和F (填”能”或”不能”)发生化学反应
(4)反应⑤的化学方程式是 。
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
将分别通入下列种溶液中,有关说法正确的是( )
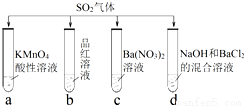
A、试管a中实验可以证明具有漂白性
B、试管b中溶液褪色,说明具有强氧化性
C、试管c中能产生白色沉淀,说明具有还原性
D、试管d中能产生白色沉淀,该沉淀完全溶于稀硝酸
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
仪器中①漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃烧匙,常用于物质分离的是( )
A.①③④ B.①②⑥ C.①③⑤ D.③④⑦
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为
Fe3++Cr2+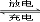 Fe2++Cr3+.下列说法一定正确的是( )
Fe2++Cr3+.下列说法一定正确的是( )

A.氧化性:Cr3+>Fe3+
B.电池放电时,负极的电极反应式为Fe2+﹣e﹣═Fe3+
C.充电时,阴极的电极反应式为Cr3++e﹣═Cr2+
D.电池放电时,Cl﹣从负极室穿过选择性透过膜移向正极室
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol·L-1和1.5 mol·L-1,
现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是
A.反应后溶液中Fe3+物质的量为0.8 mol
B.反应后产生13.44 L H2(标准状况)
C.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体
D.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:推断题
X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-半径,Y的氧化物是形成酸雨的主要物质之一。
请回答:
(1)Q元素在周期表中的位置
(2)将这五种元素原子半径从大到小排列,排在第三的元素原子是 (填元素符号)
(3)元素的非金属性Z Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有 (填序号)
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4) X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,写出A的电子式 ;B的水溶液不呈中性的原因 (用离子方程式表示)
(5) 液态A类似X2Z能微弱电离且产生电子数相同的两种离子,则液态A的电离方程式为
(6)若使A按下列途径完全转化为F:
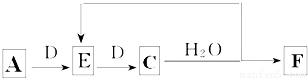
①F的化学式为 ;
②参加反应的A与完全转化为F时整个过程中消耗D的物质的量之比为
查看答案和解析>>
科目: 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:选择题
山梨酸是应用广泛的食品防腐剂,其结构如图,下列关于山梨酸的说法错误的是( )

A.分子式为C6H8O2
B.1mol该物质最多可与3mol Br2发生加成反应
C.可与小苏打溶液反应
D.存在顺反异构
查看答案和解析>>
科目: 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:填空题
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要。
(1)汽车内燃机工作时会引起N2和O2的反应:N2 + O2 2NO,是导致汽车尾气中含有NO的原因之一,科学家设计利用NH3在催化条件下将NOx还原成N2而排放。
2NO,是导致汽车尾气中含有NO的原因之一,科学家设计利用NH3在催化条件下将NOx还原成N2而排放。
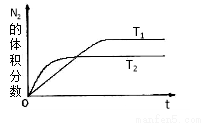
①在T1、T2温度下,一定量的NH3发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ 3H2(g) 2NH3(g)的△H_______0(填“>”或“<”)。
2NH3(g)的△H_______0(填“>”或“<”)。
②在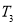 温度下,向2L密闭容器中充入10molN2与5mo1H2,50秒后达到平
温度下,向2L密闭容器中充入10molN2与5mo1H2,50秒后达到平 衡,测得NH3的物质的量为2mol,则该反应的速率v(N2)___________________。该温度下,若增大压强此反应的平衡常数将_______________(填“增大”、“减小”、“不变”或“无法确定”);若开始时向上述容器中充入N2与H2均为10 mol,则达到平衡后H2的转化率将__________。(填“升高”、“降低”)
衡,测得NH3的物质的量为2mol,则该反应的速率v(N2)___________________。该温度下,若增大压强此反应的平衡常数将_______________(填“增大”、“减小”、“不变”或“无法确定”);若开始时向上述容器中充入N2与H2均为10 mol,则达到平衡后H2的转化率将__________。(填“升高”、“降低”)
(2)利用图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
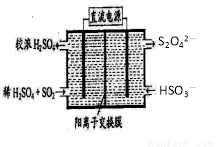
①阳极的电极反应式为_____________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应的离子方程式为 。
(3)一定条件下可用甲醇与CO反应生成醋酸消除CO污染。常温下,将a mol·L-1的醋酸与b mol L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=_________(用含a和b的代数式表示)。
L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=_________(用含a和b的代数式表示)。
查看答案和解析>>
科目: 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:填空题
下图是传统的工业生产金属铝的基本流程图。结合铝生产的流程图回答下列问题:
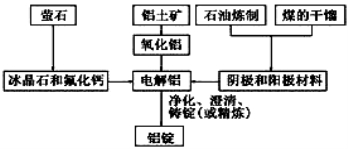
(1)工业冶炼金属铝用的是铝土矿,铝土矿的主要成分是________(填化学式)。石油炼制和煤的干馏产品__________(填物质名称)作电解铝的阴极和阳极材料。
(2)在金属铝的冶炼中加入冰晶石和氟化钙的目的是________
(3)在冶炼过程中,阳极材料需要定期进行更换,原因是氧化铝溶解并和部分冰晶石发生反应生成Al2OF62-,写出该反应的离子方程式________________。若电解的总反应为2Al2O3+3C 3CO2+4Al,则阳极的电极反应式为_______________。
3CO2+4Al,则阳极的电极反应式为_______________。
(4)冰晶石能在碱性溶液中分解,写出冰晶石与足量NaOH溶液反应生成两种钠盐的化学方程式______________。
(5)已知生产1mol铝消耗的电能为1.8x106J,9g铝制饮料罐可回收能量为0.2kJ,则铝制饮料罐的热回收效率η=_____________。(热回收效率= 回收能量/生产耗能x100%)
查看答案和解析>>
科目: 来源:2016届安徽省高三上学期12月月考化学试卷(解析版) 题型:选择题
“84”消毒液有效成分为 NaClO, 已知酸的电离平衡常数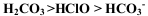 ,下列说法正确的是( )
,下列说法正确的是( )
A.“84”消毒液可以与福尔马林溶液混合使用
B.NaClO的稳定性和漂白性都比HClO强
C.工业上在特定条件下电解饱和食盐水制得NaClO,原理为:NaCl + H2O = NaClO +H2↑
D.NaClO溶液在空气中发生离子反应为: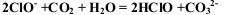
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com