
科目: 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:选择题
常温下,某溶液A中可能含有NH4+、Na+、Al3+、Fe2+、Fe3+、CO32-、SO32-、Cl-、SO42-,现取该溶液进行相关实验,实验结果如图所示:
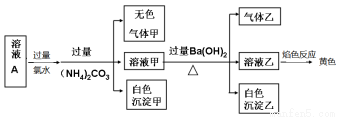
下列有关说法正确的是
A.溶液中一定有SO42-,可能有Cl-
B.溶液中一定不存在的只有Fe2+和CO32- 两种离子
C.溶液中一定存在Al3+、Na+
D.生成的甲、乙两种气体均无色,且均易溶于水
查看答案和解析>>
科目: 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:填空题
已知H2CO3的Ka1=4.2×10-7 、Ka2=5.6×10-11;HClO的Ka=3.0× 10-8,
HF的Ka=3.5×10-4 。
(1)NaClO溶液中通入少量CO2发生反应的离子方程式为 。
(2)在饱和氯水中加入NaHCO3,直至溶液的黄绿色褪去,则发生反应的离子方程式为 。
(3)常温下,将pH和体积都相同的氢氟酸和次氯酸分别加蒸馏水稀释,pH随溶液体积变化如图所示。
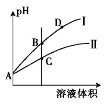
①曲线Ⅰ为 稀释时pH的变化曲线。
②取A点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗 体积较小。
(4)25 ℃时,将0.40 mol·L-1 HCN溶液与0.20 mol·L-1 NaOH溶液各100 mL混合后,测得溶液的pH=a(a>7)。则该溶液中所有离子浓度大小关系为 ;
c(HCN)-c(CN-)= mol·L-1。(假设混合后体积等于两种溶液体积之和)
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是
A.c(H+) B.Ka(HF) C. D.
D.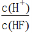
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.①② B.②④⑥ C.②③⑤ D.②④⑤⑥
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
室温下,下列溶液中粒子浓度关系正确的是
A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
B.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-)
D.CH3COONa溶液:c(Na+)>c(CH3COO-)
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
有一种酸式盐AHB,它的水溶液呈弱碱性。则以下说法:
①相同物质的量浓度的AOH溶液和H2B溶液,前者的电离程度大于后者的电离程度;
②H2B不是强酸;
③HB-的电离程度大于HB- 的水解程度;
的水解程度;
④该盐溶液的电离方程式一般写成:AHB A++HB-,HB-
A++HB-,HB- H++B2-
H++B2-
其中错误选项的组合是
A.①② B.③④ C.②③ D.①④
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:填空题
I.在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是__________。
(2)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的______H2(相同状况),则开始时反应速率的大小关系为__________,反应所需时间的长短关系是__________。
II.常温下,有浓度均为1 mol·L-1的下列四种溶液:
①H2SO4溶液 ②NaHCO3溶液 ③NH4Cl溶液 ④NaOH溶液
(1)溶液pH由大到小的顺序是______,其中由水电离的H+浓度最小的是______。(均填序号)
(2)③中各离子浓度由大到小的顺序是______ __,升高温度,NH4Cl溶液的pH (填“升高”、“降低”或“不变”)
(3)向③中通入少量氨气,此时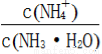 的值______(填“增大”、“减小”或“不变”)。
的值______(填“增大”、“减小”或“不变”)。
(4)将③和④混合后溶液恰好呈中性,则混合前③的体积______④的体积(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目: 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:填空题
根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25 ℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为____________。
(2)向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=__________。 ②完全沉淀后,溶液的pH=__________。
③如果向完全沉淀后的溶液中继续加入50 mL 0.001 mol·L-1的盐酸,是否有白色沉淀生成?________________(填“是”或“否”)。
(3)在某温度下,Ksp(FeS)=6.25×10-18,该温度下,FeS的溶解度为 (该温度下溶液的密度为1g/mL)
查看答案和解析>>
科目: 来源:2016届内蒙古赤峰二中高三上学期12月月考理综化学试卷(解析版) 题型:选择题
NA表示阿伏伽德罗常数的值,下列叙述错误的是( )
A.2gD216O中含有的质子数、中子数、电子数均为NA
B.78gNa2O2和Na2S的混合物中含有的Na+ 数一定为2NA
C.标准状况下,5.6LO2作氧化剂时转移电子数一定为NA
D.500mL 2mol/LNa2CO3溶液中含C微粒总数一定为NA
查看答案和解析>>
科目: 来源:2016届内蒙古赤峰二中高三上学期12月月考理综化学试卷(解析版) 题型:填空题
【选修2:化学与技术】工业上常产生大量的废气、废水、废渣、废热,如果处理不好,随意排放,会造成污染,而如果科学回收,可变废为宝。
(1)一座大型硫酸厂同时又是一座能源工厂,硫酸厂生产过程中的余热若能充分回收利用,不仅不需要外界供应能源,而且还可以向外界输出大量的热能。硫酸厂产生余热的主要设备有________。
(2)硫酸厂产生的大量烧渣(硫铁矿煅烧后的灰渣)的用途是________(写一种即可);写出电解精炼铜阳极泥的一种用途________。
(3)工业制硫酸的尾气中含有的少量SO2,可先用氨水吸收,再用稀硫酸处理。
①该反应的化学方程式为_________; ②这样处理的优点是____________________。
(4)干熄焦技术是将炼焦炉推出的约1 000℃的赤热焦炭,在熄焦室中被其逆流的冷惰性气体(主要成分是氮气,温度在170~190℃)熄灭,被加热到700~800℃的惰性气体经除尘后进入余热锅炉,产生的过热蒸气送往汽轮发电机发电。干熄1 t焦炭可产生500 kg过热蒸气,可折合成46 kg标准煤。举出两例采用逆流原理的化工设备或化学仪器________、________。
(5)下图表示石灰-石膏法吸收SO2的工艺流程,写出反应的化学方程式 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com