
科目: 来源:2015-2016学年湖北武汉第二中学高二上期中考试化学试卷(解析版) 题型:实验题
滴定实验是化学学科中重要的定量实验。 请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是______(填选项字母)
A、滴定终点读数时,俯视滴定管刻度,其他操作正确。
B、盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C、酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D、滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
滴定次数 | 待测液体积(mL) | 标准KMnO4溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 3.00 | 23.00 |
第三次 | 25.00 | 4.00 | 24.10 |
①滴定时,KMnO4溶液应装在 (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是 。
②该草酸溶液的物质的量浓度为_____________。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母)。
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉第二中学高二上期中考试化学试卷(解析版) 题型:推断题
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
Ⅰ. 将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎
Ⅱ. 采用如下装置进行电化学浸出实验
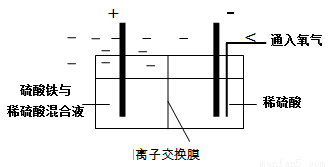
将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并 加入少量催化剂。
Ⅲ. 一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:
2RH(有机相)+ Cu2+(水相) R2Cu(有机相)+ 2H+(水相)
R2Cu(有机相)+ 2H+(水相)
分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。
Ⅳ. 电解硫酸铜溶液制得金属铜。
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S↓+ 2H+
① 阳极区硫酸铁的主要作用是 。
② 电解过程中,阳极区Fe3+的浓度基本保持不变,原因是 。
(2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解。
写出上述现象对应的反应式 。
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是 ;加入有机萃取剂的目的是 。
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是 。
(5)步骤Ⅳ,若电解200mL0.5 mol/L的CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是 。(忽略电解前后溶液体积的变化)
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:选择题
下列实验操作均要用到玻璃棒,其中玻璃棒的作用及其目的相同的是
 ① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶中转移液体
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶中转移液体
 A.①和④ B.①和③ C.①和② D.③和④
A.①和④ B.①和③ C.①和② D.③和④
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:选择题
在强酸性溶液中,下列离子组能大量共存且溶液无色透明的是
A.Ag+、Na+、Cl-、K+ B.Na+、Cu2+、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl- D.Ba2+、HCO3-、NO3-、K+
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:选择题
下列有关实验操作中,正确的是
A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道
C.用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:选择题
在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42—离子完全沉淀;如加入足量强碱并加热可得到c mol NH3,(已知NH4++OH- 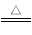 NH3↑+H2O)则原溶液中的Al3+离子浓度(mol·L-1)为
NH3↑+H2O)则原溶液中的Al3+离子浓度(mol·L-1)为
A. 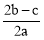 B.
B. 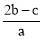 C.
C. 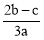 D.
D. 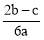
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:选择题
如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比可能为

A.7:2 B.5:4
C.3:5 D.2:7
查看答案和解析>>
科目: 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:推断题
(1)已知4℃时四种化合物在水中和液氨中的溶解度如下表:
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O(l) | 170g | 9.20g | 1.50×10-4g | 33.3g |
NH3(l) | 86.0g | 97.2g | 0.80g | 0.01g |
①上述四种物质能在水中发生的复分解反应的离子方程式为 ;
②上述四种物质能在液氨中发生的复分解反应的化学方程式为 ;
(2)完成下列反应的离子方程式:
①碳酸氢铵溶液与少量的烧碱溶液反应: ;
②20毫升0.1mol/L碳酸氢钙溶液与56毫升0.05mol/L氢氧化钠溶液反应: ;
③石灰乳与少量的碳酸氢钠溶液反应: ;
查看答案和解析>>
科目: 来源:2015-2016学年山西忻州第一中学高二上期中考试化学试卷(解析版) 题型:选择题
在常温下,把一个盛有一定量甲烷和氯气的密闭玻璃容器放置在漫散光的地方,两种气体发生反应后恢复到原温度。下列叙述中不正确的是
A.容器内原子总数不变
B.容器内分子总数不变
C.容器内压强不变
D.反应后得到的产物为混合物
查看答案和解析>>
科目: 来源:2015-2016学年山西忻州第一中学高二上期中考试化学试卷(解析版) 题型:选择题
在密闭容器中,A和B反应生成C,其反应速率分别用v(A)、v (B)、v (C)表示,已知它们之间的如下关系:3v (A)=2v (B),3v (C)=2v (B)。则此反应可表示为
A.3A+2B = 2C B.2A+3B = 2C C.3A+ 2B = 3C D.A + B = C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com