
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.酸性高锰酸钾与少量双氧水反应:2MnO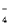 +7H2O2+6H+= 2Mn2++6O2↑+10H2O
+7H2O2+6H+= 2Mn2++6O2↑+10H2O
B.用石墨电极电解饱和MgCl2溶液:2Cl-+ 2H2O 2OH-+ Cl2↑+ H2↑
2OH-+ Cl2↑+ H2↑
C.Mg(HCO3)2溶液与过量的NaOH溶液反应:Mg2++ HCO3-+OH—=MgCO3↓+H2O
D.向NaClO溶液中通入过量CO2;CO2+ClO—+H2O=HCO3-+HClO
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:选择题
某同学组装了图所示的电化学装置,其中电极Ⅰ为Al,其它均为Cu,下列说法正确的是
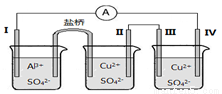
A.装Al2(SO4)3 溶液的烧杯是原电池,其余两个为电解(电镀)池
B.盐桥中电子从右侧流向左侧
C.电极Ⅱ逐渐溶解
D.电极IV的电极反应:Cu2+ + 2e- = Cu
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:选择题
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是
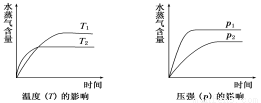
A.CO2(g)+2NH3(g)  CO(NH2)2(s)+H2O(g);ΔH<0
CO(NH2)2(s)+H2O(g);ΔH<0
B.CO2(g)+H2(g)  CO(g)+H2O(g);ΔH>0
CO(g)+H2O(g);ΔH>0
C.CH3CH2OH(g)  CH2==CH2(g)+H2O(g);ΔH>0
CH2==CH2(g)+H2O(g);ΔH>0
D.2C6H5CH2CH3(g)+O2(g)  2C6H5CH=CH2(g)+2H2O(g);ΔH<0
2C6H5CH=CH2(g)+2H2O(g);ΔH<0
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:选择题
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1 的稀氨水滴定得下图。下列说法正确的是
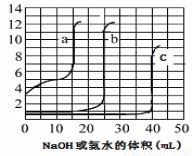
A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞做指示剂
D.由图可知滴定前醋酸电离度约为1.67﹪
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:选择题
已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等。为了进一步探究该水溶液的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰。
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③另取溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,以下推测正确的是
A.无法确定溶液中是否存在Cu2+离子
B.原溶液中不含K+、Al3+、CO32-等离子
C.根据步骤②只能确定溶液中一定存在NO3-离子
D.步骤③所得到的白色沉淀共有2种钡盐
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:填空题
向炭粉、Cu和Fe2O3组成的混合粉末中加入一定量的稀硫酸,充分反应后过滤,得到溶液A,将沉淀物洗涤、干燥,得到固体B。
(1)碳的原子结构示意图为 ,氧元素在周期中的位置是
(2)加入稀硫酸后,发生反应的离子方程式 ,溶液A中一定存在的金属阳离子是 。
(3)关于固体B的成分,下列选项中可能的有 。
A.炭粉
B.炭粉和Cu
C.炭粉和Fe2O3
D.Cu和Fe2O3
E.炭粉、Cu和Fe2O3
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:填空题
某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)生成甲的化学反应方程式为
(2)甲与水反应可得H2,其化学方程式是 。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是 ;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是 。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料) 。
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:推断题
无机化合物A和金属B是中学化学常见的固体,其中A显淡黄色。相同质量的A、B都能与液体C反应放出气体,两气体又能恰好完全反应生成C。利用B在高温下的挥发性,可通过它的碳酸盐和焦炭在真空环境中来制备B。化合物D可作为有机反应中的脱氢试剂,1molD和1mol NH4Cl反应生成2mol气体E和1molB的氯化物。已知标准状况下气体E的密度为0.76g·L-1。
请回答下列问题:
(1)E的化学式为
(2)题中制备B的化学方程式为 下列物质能替代焦炭的是 。
A.Na B.H2 C.KMnO4 D.Cl2
(3)B与E在一定条件下 (填“可能”或“不可能”)直接发生反应产生D,判断理由是 。
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:填空题
某研究小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱(Na2CO3)和氯化铵(NH4Cl)。

已知盐的热分解温度:NH4HCO3 36℃;NaHCO3 270℃;NH4Cl 340℃;Na2CO3>850℃
请回答:
(1)从NaCl溶液到沉淀1的过程中,需蒸发浓缩。在加入固体NH4HCO3之前进行蒸发浓缩优于在加入NH4HCO3固体之后,其原因是 。
(2)为提高NH4Cl产品的产率和纯度,需在滤液1中加入氨水,理由是 ;步骤X包括的操作有 。
(3)测定NH4Cl产品的纯度时,可采用的方法:在NH4Cl溶液中加入甲醛使之生成游离酸(4NH4Cl+6HCHO=(CH2)6N4+4HCl+6H2O),然后以酚酞为指示剂,用NaOH标准溶液(需用邻苯二甲酸氢钾基准物标定)进行滴定。
①下列有关说法正确的是
A.为了减少滴定误差,滴定管、锥形瓶均须用待装液润洗
B.标准NaOH溶液可以装入带有耐腐蚀旋塞的玻璃滴定管中
C.开始滴定前,不需擦去滴定管尖悬挂的液滴
D.三次平行测定时,每次需将滴定管中的液面调至“0”刻度或“0”刻度以下的附近位置
②若用来标定NaOH标准溶液的邻苯二甲酸氢钾基准物使用前未烘至恒重,则测得NH4Cl产品的含量比实际含量 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:填空题
氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得。实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75∶2);②在碳存在下,X与N2反应生成AlN。请回答:
(1)X的化学式为 。
(2)碳热还原制备氮化铝的总反应化学方程式为:
Al2O3(s)+3C(s)+N2(g) 2AlN(s)+3CO(g)
2AlN(s)+3CO(g)
①在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如下图曲线甲所示。下列说法不正确的是 。
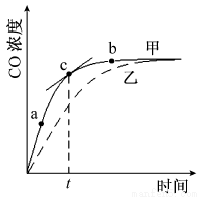
A.从a、b两点坐标可求得从a到b时间间隔内该化学反应的平均速率
B.c点切线的斜率表示该化学反应在t时刻的瞬时速率
C.在不同时刻都存在关系:v(N2)=3v(CO)
D.维持温度、容积不变,若减少N2的物质的量进行反应,曲线甲将转变为曲线乙
②一定温度下,在压强为p的反应体系中,平衡时N2的转化率为α,CO的物质的量
浓度为c;若温度不变,反应体系的压强减小为0.5p,则N2的平衡转化率将 α (填“<”、“=”或“>”),平衡时CO的物质的量浓度
A.小于0.5c B.大于0.5c,小于c
C.等于c D.大于c
③该反应只有在高温下才能自发进行,则随着温度升高,反应物Al2O3的平衡转化率将 (填“增大”、 “不变”或“减小”),理由是 。
(3)在氮化铝中加入氢氧化钠溶液,加热,吸收产生的氨气,进一步通过酸碱滴定法可以测定氮化铝产品中氮的含量。写出上述过程中氮化铝与氢氧化钠溶液反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com