
科目: 来源:2016届新疆兵团农二师华山中学高三上学期第二次月考化学试卷(解析版) 题型:实验题
氯化铁是常见的水处理剂。某氯化铁(FeCl3•6H2O)样品含有少量FeCl2杂质。现要测定其中FeCl3•6H2O的质量分数,实验按以下步骤进行:

已知有关离子方程式为:2Fe3++2I-═2Fe2++I2,I2+2S2O32-═2I-+S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:________________________。
(2)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、_________(填仪器名称)。
(3)操作II必须用到的仪器是________(选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是__________________________。
(4)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3溶液18.00mL。该样品中FeCl3•6H2O(式量为270.5)的质量分数为_____________。
(5)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是________(选填编号)。
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品元素的含量,完成下列填空。
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是________;在过滤前,需要检验是否沉淀完全,其操作___________________;判断是否恒重的标准是_________________________。
查看答案和解析>>
科目: 来源:2016届四川省雅安市高三上学期11月月考理综化学试卷(解析版) 题型:选择题
常温下,下列各组离子或分子在指定溶液中能大量共存的是
A. pH=l的溶液中:Fe2+、Na+、SO42-、NO3-
B.水电离的c(H+)=l×l0-13mol/L的溶液中:NH4+、K+、Cl-、HCO3-
C. KMnO4溶液中:H+、Na+、SO42-、C2H5OH
D. 使甲基橙变红色的溶液中:NH4+、Al3+、NO3-、Cl-
查看答案和解析>>
科目: 来源:2016届四川省雅安市高三上学期11月月考理综化学试卷(解析版) 题型:选择题
在一定温度下,将6 mol CO2和8 mol H2充入2L恒容密闭容器中,发生反应:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是
CH3OH(g)+H2O(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是
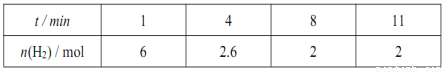
A.反应前4min的平均速率v(CO2)= 0.45 mol/(L.min)
B.达到平衡时,H2的转化率为25%
C.其他条件不变,升高温度,反应达到新平衡时CH3OH的体积分数增大
D.该温度下,该反应的平衡常数为0.5
查看答案和解析>>
科目: 来源:2016届四川省雅安市高三上学期11月月考理综化学试卷(解析版) 题型:填空题
高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,工业上用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体的过程为:
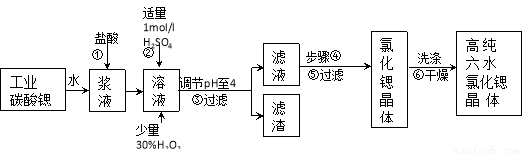
已知: Ⅰ. SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
(1)操作①加快反应速率的措施有 (写一种)。碳酸锶与盐酸反应的离子方程式 。
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为 。
(3)在步骤②-③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为________________。
A.氨水 B.氢氧化锶粉末 C. 氢氧化钠 D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是 (填化学式)。
(5)步骤④的操作是 、 。
(6)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
查看答案和解析>>
科目: 来源:2016届山西省晋中市四校高三上学期期中联考化学试卷(解析版) 题型:选择题
某学生鉴定甲盐的流程如图所示,下列说法正确的是
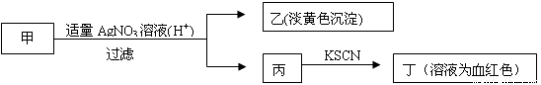
A.如果甲中含有S2-,则乙是硫磺沉淀
B.如果乙是AgCl沉淀,那么甲是FeCl3
C.丙中肯定含有Fe3+,所以甲是FeBr2
D.甲中含有铁元素。可能显示+2或者+3价
查看答案和解析>>
科目: 来源:2016届山西省晋中市四校高三上学期期中联考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 (s) + 2Fe3+(aq) = 2Fe(OH)3 (s) + 3Mg2+(aq)
B.钠与CuSO4溶液反应:2Na + Cu2+ = Cu↓ + 2Na+
C.已知:酸的强弱H2CO3>HClO>HCO3-,则:2ClO-+ CO2(少量) + H2O=CO32-+ 2HClO
D.将足量的NaHCO3溶液加入少量澄清石灰水中:Ca2+ + OH- + HCO3-=CaCO3↓ + H2O
查看答案和解析>>
科目: 来源:2016届山西省晋中市四校高三上学期期中联考化学试卷(解析版) 题型:选择题
稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:①铈常见的化合价为+3和+4;②氧化性:Ce4+>Fe3+。下列说法正确的是
A.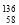 Ce、
Ce、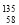 Ce、
Ce、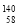 Ce、
Ce、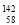 Ce它们互称为同素异形体
Ce它们互称为同素异形体
B.铈溶于氢碘酸的主要化学方程式可表示为2Ce+6HI=2CeI3+3H2↑
C.工业上可以采用电解氯化铈水溶液来获得铈单质
D.工业上金属铈一般保存在敞口容器中
查看答案和解析>>
科目: 来源:2016届山西省晋中市四校高三上学期期中联考化学试卷(解析版) 题型:填空题
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为______ ____,Fe3O4可写成FeO·Fe2O3的形式,如果将Pb3O4也写成相对应的形式应为:______________
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________。PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为______________。
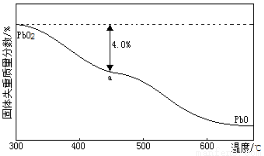
(3)PbO2在加热过程发生分解的失重曲线如右图所示,已知失重曲线上的a点为样品失重4.0%(即 ×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n_______________,____________。
×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n_______________,____________。
查看答案和解析>>
科目: 来源:2016届山西省晋中市四校高三上学期期中联考化学试卷(解析版) 题型:实验题
某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:
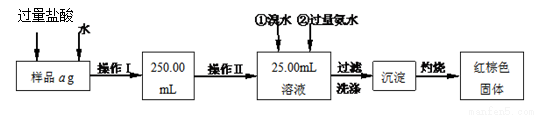
Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、________,(填仪器名称)。
(2)请写出加入溴水发生的离子反应方程式___________________________________。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是 _;若蒸发皿质量是w1 g,蒸发皿与加热后固体总质量是w2 g,则样品中铁元素的质量分数是____ _。
Ⅱ.有同学提出,还可以采用以下方法来测定:
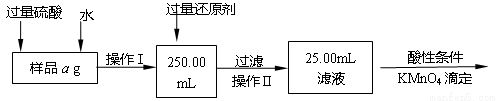
(1)溶解样品改用了硫酸,而不再用盐酸,为什么?_____________________。
(2)选择的还原剂是否能用铁__________(填“是”或“否”),原因是:____________。
(3)若滴定用掉c mol/L KMnO4溶液b mL,则样品中铁元素的质量分数是____________。
查看答案和解析>>
科目: 来源:2016届山东省烟台市高三上学期期中测试化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.为防止水污染,可用O3替代Cl2作饮用水消毒剂
B.实验室可用浓硫酸干燥SO2气体
C.16O和18O能形成三种化学性质相同的氧分子
D.Al2(SO4)3,可除去碱性废水及酸性废水中的悬浮颗粒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com