
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某期刊封面上一个分子球棍模型图如图所示,图中“棍”代表单键、双键或三键,不同颜色的球代表不同元素的原子。该模型图可代表一种

A.醇 B.酸 C.酯 D.氨基酸
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某高校研究课题组利用生物发酵技术生产灵芝酸单体的分子结构图如右图所示,下列关于该有机物的说法不正确的是
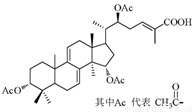
A.能与Br2发生加成反应
B.能发生酯化反应
C.能发生水解反应
D.分子中有7 个手性碳原子
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
CoCl2(g)  CO(g)+Cl2(g) △H>0,当反应达到平街时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体。能提高CoCl2转化率的是
CO(g)+Cl2(g) △H>0,当反应达到平街时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体。能提高CoCl2转化率的是
A. ①②④ B. ①④⑥ C. ②③⑤ D. ③⑤⑥
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:实验题
50mL0.50 mol·L-1盐酸与50mL0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)右图装置名称为____,图中尚缺少的一种玻璃用品名称是_____。

(2)烧杯间填满碎纸条的作用是_______。
(3)实验中改用60mL0.50 mol·L-1盐酸与50mL0.55 mol·L-1NaOH溶液进行反应,与上述实验相比较,所放出的热量_____(填“相等”或“不相等”),中和热______(填“相等”或“不相等”),理由是______。
(4)用相同浓度和体积的氨水代替NaOH 溶液进行上述实验,测得中和热的数值与57.3kJ / mol 相比较会_____。(填“偏大”“偏小”或“无影响”)。
(5)完整地做一次这样的实验,需测定___次温度。
(6)大烧杯上如不盖硬纸板,求得的中和热数值____(填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目: 来源:2014-2015学年四川省高三化学一诊模拟理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.1 mol CH4含有的电子数为NA
B.标准状况下,22.4 L 己烷中共价键数为19NA
C.6.4 g CaC2固体中所含阴离子数为0.2 NA
D.1 L 1 mol/L的NaHCO3 溶液中含有NA 个HCO3-
查看答案和解析>>
科目: 来源:2014-2015学年四川省高三化学一诊模拟理综化学试卷(解析版) 题型:选择题
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素, 它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法不正确的是
A.原子半径W>X>Y B.W2Y的电子式为: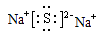
C.元素的金属性W<X D.W2Y2中既有离子键,又有共价键
查看答案和解析>>
科目: 来源:2014-2015学年四川省高三化学一诊模拟理综化学试卷(解析版) 题型:简答题
(1)利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸。
已知:①N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
②N2(g)+3H2(g) 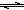 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
③2H2(g)+O2(g) = 2H2O(g) △H=-483.6 kJ/mol
氨催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为 。
(2)研究在其他条件不变时,改变起始物氢气的物质的量对N2(g)+3H2(g) 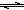 2NH3(g)反应的影响实验结果如图所示(图中T表示温度,n表示物质的量):
2NH3(g)反应的影响实验结果如图所示(图中T表示温度,n表示物质的量):

①图像中T2和T1的关系是:T2 T1(填“高于”“低于”“等于”“无法确定”)。
②a、b、c三点中,N2转化率最高的是 (填字母)。
③若容器容积为1L,T2℃在起始体系中加入1 mol N2 ,n(H2)=3mol,经过5 min反应达到平衡时H2的转化率为60%,则v(NH3)= 。保持容器体积不变,若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则Q___110.88 kJ(填“>”、“<”或“=”)。
查看答案和解析>>
科目: 来源:2016届河北邯郸第一中学高三一轮收官考试一理综化学卷(解析版) 题型:选择题
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
A.常温下28g乙烯中所含极性键的数目为4NA
B.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NAFe3+
C.标准状况下,22.4L甲醇中所含羟基数为NA
D.10LpH=1的硫酸溶液中含有的H离子数为2NA
查看答案和解析>>
科目: 来源:2016届河北邯郸第一中学高三一轮收官考试一理综化学卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如表所示:
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5.+3.-3 | -2 |
下列叙述正确的是( )
A.X、Y元素的金属性:X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
科目: 来源:2016届河北邯郸第一中学高三一轮收官考试一理综化学卷(解析版) 题型:简答题
工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外.还含有少量NH4+、Fe3+、AsO43-、Cl-。为除去杂质离子,部分操作流程如下:
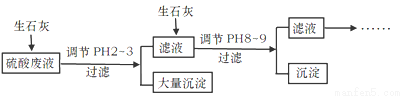
请回答问题:
(1)NH4+在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在.现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH4+)恰好是NH4Cl溶液中c(NH4+)的2倍,则c[(NH4)2SO4]_____c(NH4Cl)(填:<、= 或 >) 。
(2)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中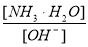 ______(填“增大”、“减小”或“不变”)。
______(填“增大”、“减小”或“不变”)。
(3)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4·2H2O[含有少量Fe(OH)3],提纯CaSO4·2H2O的主要步骤:向沉淀中加入过量_______,充分反应后,过滤、洗涤、______。
(4)25℃,H3AsO4电离常数为K1=5.6×10-3、K2=1.7×10-7、K3=4.0×10-12。当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2.
①pH调节到8左右Ca3(AsO4)2 才开始沉淀的原因是________。
② Na3AsO4 第一步水解的平衡常数数值为:________。
③已知:AsO43-+2I-+2H+= AsO43-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+ 。上述两个反应中还原性最强的微粒是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com