
科目: 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
已知:①C(s)+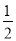 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH=-393.51 kJ·mol-1
计算反应C(s)+CO2(g)=2CO(g)的反应热ΔH的值为
A.-283.01 kJ·mol-1 B.+172.51 kJ·mol-1
C.+283.1 kJ·mol-1 D.+504.00 kJ·mol-1
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:填空题
用编号填空:
(1)下列关于燃烧热的说法正确的是
A.101kPa时1mol氢气完全燃烧生成水蒸气所放出的热量即氢气的燃烧热;
B.101kPa时1mol碳在氧气中燃烧生成CO所放出的热量即碳的燃烧热;
C.某物质的燃烧热不随热化学方程式计量数的改变而改变。
(2)下列关于用稀盐酸和氢氧化钠稀溶液测中和热的说法错误的是
A.实验结果随反应物用量改变而改变;
B.实验中氢氧化钠溶液稍过量是为了使盐酸完全被氢氧化钠中和;
C.实验中不可用环形铜质搅拌棒代替环形玻璃搅拌棒。
(3)下列关于化学平衡的说法错误的是
A.若改变影响化学平衡的条件之一,平衡向能够使这种改变减弱的方向移动;
B.达到化学平衡时,各组分的浓度不再改变,反应停止;
C.化学平衡移动,化学平衡常数不一定改变。
(4)改变下列条件,化学平衡一定向正反应方向移动的是
A.增大反应物浓度 B.升高温度 C.增大压强
(5)下列关于电解质的说法错误的是
A.酸、碱、盐及氧化物都是电解质;
B.电解质溶液能导电是因为发生了电离,产生了自由移动的离子;
C.电解质不一定能导电,能导电的物质不一定是电解质。
(6)下列反应的△H<0的是
A.铝和稀硫酸反应 B.碳酸氢铵受热分解 C.氢氧化钡晶体与氯化铵晶体反应
(7)下列情况,均为日常生活中为了改变反应速率而采取的措施,其中不属于浓度影响反应速率的是
A.汽车加大油门 B.食物放冰箱 C.糕点包装袋里放小包除氧剂
(8)下列实验现象与实际不符的是
A.向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色;
B.浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊;
C.将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅。
(9)一定温度下,有三种酸:A.盐酸,B.硫酸,C.醋酸,回答下列问题:
①三种酸溶液等物质的量浓度时,c(H+)最大的是 ;
②三种酸的c(H+)相同时,溶液浓度最大的是 ;
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,再加入同样的锌粒,反应最快的是 。
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:填空题
(1)当1g氨气完全分解为N2和H2时,吸收2.7kJ的热量,写出其热化学方程式: 。
(2)HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和NaOH反应的中和热的热化学方程式为 。
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:填空题
在密闭容器中,使3 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g)  2NH3(g) ΔH<0。已知平衡时NH3为nmol。回答下列问题:
2NH3(g) ΔH<0。已知平衡时NH3为nmol。回答下列问题:
(1)上述平衡中,N2和NH3的浓度比= (用含n的代数式表示);N2和H2的转化率之比=________。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量________,密度___________ (填“变大”、“变小”或“不变”) 。
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,达到新平衡后,容器内温度________(填“>”、“<”或“=”)原来的2倍。
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:填空题
乙苯催化脱氢制苯乙烯反应:

(1)已知:
化学键 | C-H | C-C | C=C | H-H |
键能/kJ·molˉ1 | 412 | 348 | 612[ | 436 |
计算上述反应的△H=____________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________(用含α等字母的代数式表示)。
查看答案和解析>>
科目: 来源:2015-2016学年河南省高一上学期二次月考化学试卷(解析版) 题型:选择题
下列四幅图中,小白球代表的是氢原子,大灰球代表的是氦原子。最适合表示同温同压下,等质量的氢气与氦气的混合气体的图示是
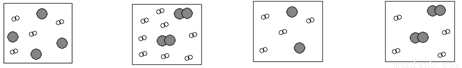
A B C D
查看答案和解析>>
科目: 来源:2015-2016学年河南省高一上学期二次月考化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式正确的是
A.用小苏打治疗胃酸过多:HCO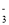 +H+=CO2↑+H2O
+H+=CO2↑+H2O
B.往碳酸镁中滴加稀盐酸:CO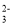 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
C.往澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
D.氢氧化钡溶液与稀硫酸反应: Ba2++SO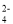 +H++OH-=BaSO4↓+H2O
+H++OH-=BaSO4↓+H2O
查看答案和解析>>
科目: 来源:2015-2016学年河南省高一上学期二次月考化学试卷(解析版) 题型:选择题
酸性条件下20mL 0.5mol/L的KMnO4溶液可将25 mL 2 mol/L的FeSO4溶液中的Fe2+恰好完全氧化为Fe3+,则KMnO4被还原的产物是
A.K2MnO4 B.Mn2O3 C.MnO2 D.Mn2+
查看答案和解析>>
科目: 来源:2015-2016学年河南省高一上学期二次月考化学试卷(解析版) 题型:选择题
下列关于物质的量浓度表述正确的是
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO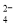 总物质的量为0.6mol
总物质的量为0.6mol
B.50mL2mol·L-1NaCl溶液和100mL0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C.用1L水吸收22.4L氯化氢所得盐酸的浓度是1mol·L-1
D.10g98%的硫酸(密度为1.84g·cm-3)与10mL18.4mol·L-1的硫酸的浓度是相同的
查看答案和解析>>
科目: 来源:2015-2016学年河南省高一上学期二次月考化学试卷(解析版) 题型:选择题
下列各组反应,前后均可以用同一个离子方程式表示的是
A.HCl+Na2CO3 HCl+NaHCO3
B.HCl+Na2CO3 H2SO4+K2CO3
C.H2S+NaOH H2SO4+KOH
D.BaCl2+Na2SO4 BaCO3+H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com