
科目: 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:选择题
下列除杂操作可行的是
A.通过浓硫酸除去HCl中的H2O B.通过灼热的CuO除去H2中的CO
C.通过灼热的镁粉除去N2中的O2 D.通过水除去CO中的CO2
查看答案和解析>>
科目: 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:选择题
将足量的CO2不断通入KOH、Ca(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
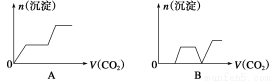

查看答案和解析>>
科目: 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:填空题
(1)写出下列物质的化学式:硫铁矿 石膏
(2)SiO2是硅最重要的化合物,其用途是 (举一例)
(3)已知1g乙醇完全燃烧生成液态水放出29.7kJ的热量,写出乙醇燃烧热的热化学方程式 。
(4)配平化学方程式:___K2Cr2O7+___HCl——___KCl+___CrCl3+___Cl2↑+___H2O
查看答案和解析>>
科目: 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:填空题
硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下:
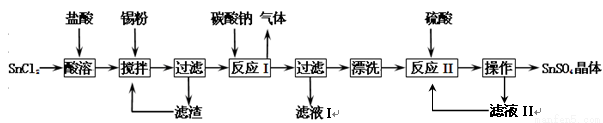
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
III.Sn(OH)2的性质与Al(OH)3性质相似。请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,这样操作的原因是 。
(2)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子方程式是 。
(3)将反应I滤液中的溶质提取出来的操作是 ,滤液I溶质的成分是 。
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
(5)称取SnSO4·x H2O晶体50.2g,在隔绝空气的情况下小火加热至结晶水全部失去,冷却称量固体质量为43g,列式计算该晶体的化学式为 。
查看答案和解析>>
科目: 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=14的溶液中:K+、NH4+、NO3-、HCO3-
B.澄清透明的溶液:Cu2+、Mg2+、SO42-、Cl-
C.0.1mol·L-1Fe(NO3)2溶液中:H+、Ca2+、SCN-、Cl-
D.c(Fe2+)=1.0 mol·L-1溶液:H+、K+、Cl-、MnO4-
查看答案和解析>>
科目: 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.Fe2O3溶于HI溶液中:Fe2O3 + 6H+ =2Fe3++ 3H2O
B.碳酸钠的水【解析】
CO32-+ 2H2O H2CO3 + 2OH-
H2CO3 + 2OH-
C.硫酸铝溶液中滴加过量浓氨水:Al3++4NH3·H2O===AlO +4NH4++2H2O
+4NH4++2H2O
D.用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+ =I2 +2H2O
查看答案和解析>>
科目: 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2,CuSO4•5H2O受热分解的化学方程式为:CuSO4•5H2O(s) CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
A.△H2>△H3 B.△H1<△H3 C.△H1+△H3=△H2 D.△H1+△H2>△H3
查看答案和解析>>
科目: 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
向20mL 0.1mol/L NH4HSO4溶液中滴入0.1mol/L NaOH溶液至恰好反应完全,下列说法正确的是
A.整个反应过程中:c(H+) + c(Na+) + c(NH4+)=c(OH-) + 2c(SO42-)
B.当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)= c(OH-)
C.当滴入20mL NaOH溶液时:2c(SO42-)=c(NH3·H2O)+ c(NH4+)
D.当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:填空题
钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。
(1)CoxNi(1-x)Fe2O4(其中Co、Ni均为+2)可用作H2O2分解的催化剂,具有较高的活性。
①该催化剂中铁元素的化合价为 ;
②图1表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是 ;
(2)草酸钴是制备钴的氧化物的重要原料。下图2为二水合草酸钴(CoC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
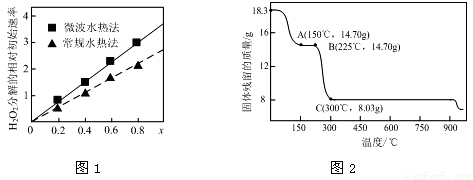
①通过计算确定C点剩余固体的化学成分为 (填化学式)。试写出B点对应的物质与O2在225℃~300℃发生反应的化学方程式: 。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比。
查看答案和解析>>
科目: 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:填空题
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。
(1)Fe基态核外电子排布式为 。
(2)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的第一电离能由大到小的顺序为 。
(3)与OCN-互为等电子体的一种分子为 (填化学式)
(4)铁元素还能与一些氨基酸形成配合物,羧基中碳原子的杂化类型是 ;1mol乙酸中含有σ键的数目为 。
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。该合金的化学式为 。
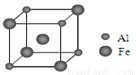
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com