
科目: 来源:2016届陕西省西安市高三上学期10月月考化学试卷(解析版) 题型:选择题
X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z- ,Y+和Z-离子具有相同的电子层结构。下列说法正确的是
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z- D.原子半径:Y>X>Z
查看答案和解析>>
科目: 来源:2016届陕西省西安市高三上学期10月月考化学试卷(解析版) 题型:选择题
某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g) 3Z(g),平衡时, X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时, X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4 mol·L-1
查看答案和解析>>
科目: 来源:2016届陕西省西安市高三上学期10月月考化学试卷(解析版) 题型:选择题
已知I﹣、Fe2+、SO2和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Fe2+<H2O2<I﹣<SO2,则下列反应不能发生的是
A.2Fe3++SO2+2H2O═2Fe2++SO42﹣+4H+
B.H2O2+H2SO4═SO2+O2+2H2O
C.I2+SO2+2H2O═H2SO4+2HI
D.2Fe3++H2O2═2Fe2++O2↑+2H+
查看答案和解析>>
科目: 来源:2016届陕西省西安市高三上学期10月月考化学试卷(解析版) 题型:填空题
X、Y、Z、M、G五种元素分属三个短周期;且原子序数依次增大。X、Z同主族;可形成离子化合物ZX;Y、M同主族;可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式);非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 (写出其中两种物质的化学式)。
(4)X2M的燃烧热ΔH =-a kJ·mol-1;写出X2M燃烧反应的热化学方程式: 。
(5)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
(6)熔融状态下;Z的单质和FeG2能组成可充电电池(装置示意图如下);反应原理为2Z+FeG2 Fe+2ZG
Fe+2ZG

放电时;电池的正极反应式为 ;充电时; (写物质名称)电极接电源的负极:该电池的电解质为
查看答案和解析>>
科目: 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
NA代表阿伏伽德罗常数,下列叙述正确的是
A.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
B.1molFe与过量的稀HNO3反应,转移的电子数为2 NA
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.一定温度下,l L 0.50 mol•L﹣1NH4C1溶液与2 L0.25mol•L﹣1NH4C1溶液NH4+的离子数均为0.5NA
查看答案和解析>>
科目: 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列有关溶液组成的描述合理的是
A.由水电离出的c(H+)=10﹣13mol•L﹣1的溶液中可能存在:HCO3﹣、K+、Na+、Cl﹣
B.酸性溶液中可能大量存在Na+、ClO﹣、SO42﹣、I﹣
C.含有0.1 mol•L﹣1 Fe3+的溶液中可以大量存在:K+、Mg2+、I﹣、NO3﹣
D.室温下,pH=l的溶液中一定可以存在:Na+、Fe3+、NO3﹣、SO42﹣
查看答案和解析>>
科目: 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
常温下,向l00mL 0.01mol•L﹣1HA溶液中逐滴加入0.02mol•L﹣1MOH溶液,如图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,正确的是
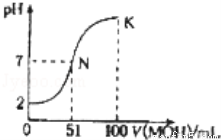
A.HA为一元强酸,MOH为一元强碱
B.K点所示溶液中c(A﹣)>c(M+)
C.N点水的电离程度小于K点水的电离程度
D.K点溶液的pH=10,则有c(MOH)+c(OH﹣)﹣c(H+)=0.005mol•L﹣1
查看答案和解析>>
科目: 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列实验现象预测或装置的选用正确的是

A.用装置(Ⅰ)加热草酸晶体的方法获取某些气体(草酸晶体的熔点101.5℃,分解温度约为150℃)
B.用装置(Ⅱ)进行实验时,酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C.用装置(Ⅲ)进行实验时,广口瓶内先有浅红棕色气体出现后又变为无色,且不会产空气污染
D.用装置(Ⅳ)分离溴苯和苯的混合物
查看答案和解析>>
科目: 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:填空题
铁及其化合物在生产、生活中有广泛应用,请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) 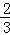 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数 如下:
温度/℃ 1000 1115 1300
平衡常数 4.0 3.7 3.5
(1)该反应的平衡常数表达式K= ;△H 0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是 .
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正 υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)= .
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是 ;生成0.5mol K2FeO4转移电子的物质的量是 mol.
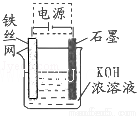
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为 .
查看答案和解析>>
科目: 来源:2016届山东省临沂市高三上学期第一次月考化学试卷(解析版) 题型:选择题
被称为万能还原剂的NaBH4溶于水并和水发生如下反应:
NaBH4+H2O = H2↑+NaBO2(未配平,其中NaBH4中氢元素为﹣1价),则下列说法正确的是
A.被氧化元素与被还原元素的质量比为1:1
B.NaBH4是氧化剂,H2O是还原剂
C.硼元素被氧化,氢元素被还原
D.NaBH4既是氧化剂,又是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com