
科目: 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列反应所得溶液中一定只含一种溶质的是
A.向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液
B.向稀硝酸中加入铁粉
C.向稀盐酸中滴入少量的NaAlO2溶液
D.向NaOH溶液中通入CO2气体
查看答案和解析>>
科目: 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3 = bO2↑+ c Cl2↑+ d HClO4 + e H2O。下列有关说法不正确的是
A.由反应可确定:氧化性HClO3>O2
B.由非金属性Cl>S,可推知酸性HClO3>H2SO4
C.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O
D.若化学计量数a=8,b=3,则该反应转移电子数为20e-
查看答案和解析>>
科目: 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法中正确的是
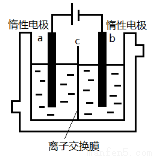
A.电解过程中OH-从a极区通过离子交换膜c进入b极区
B.随着电解进行,KOH溶液浓度会逐渐减小
C.当阳极有0.1mol I-放电时,阴极生成6.72LH2
D.a电极反应式:I- -6e-+6OH-=IO3-+3H2O,a极区的KI最终转变为KIO3
查看答案和解析>>
科目: 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:填空题
Ⅰ(1)CO可用于炼铁,已知Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g) ΔH 1=+489.0 kJ·mol-1,C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
Ⅱ(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:负极的电极反应式是 。
(3)下图是一个电化学过程示意图。
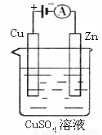
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
查看答案和解析>>
科目: 来源:2016届山东省青岛市高三上学期10月月考化学试卷(解析版) 题型:选择题
分类法在化学研究中起到了非常重要的作用。下列对物质的分类正确的组合是
①酸性氧化物:CO2、SO2、SiO2
②混合物:漂白粉、氨水、铝热剂
③电解质:氯气、硫酸钡、酒精
④同位素:12C、14C与14N
⑤同素异形体:C60、金刚石、石墨
⑥胶体:豆浆、硅酸、食盐水
A.只有①②④ B.只有②③④ C.只有①②⑤ D.只有②⑤⑥
查看答案和解析>>
科目: 来源:2016届山东省青岛市高三上学期10月月考化学试卷(解析版) 题型:选择题
室温下,下列各组离子在指定溶液中可以大量共存的是
A.pH=12的溶液:Ca2+、NH4+、Br-、HSO3-
B.无色溶液:K+、A13+、HCO3—、C1—
C.通入H2 S无沉淀:Cu2+、Na+、I—、SO42—
D.c(H+)=1×10—2 mol/L的溶液:Fe3+、Ba2+、NO3-、Cl—
查看答案和解析>>
科目: 来源:2016届山东省青岛市高三上学期10月月考化学试卷(解析版) 题型:选择题
a mol FeS与b mol FeO投入到V L c mol·L-1的硝酸溶液中,恰好完全反应,还原产物只有NO,所得澄清溶液可看作是Fe(NO3)3与H2SO4的混合液,则反应中未被还原的硝酸可能为
①(a+b)×63g ;②(a+b)×189g;③(a+b)mol ;④(V•c—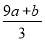 )mol
)mol
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目: 来源:2016届山东省青岛市高三上学期10月月考化学试卷(解析版) 题型:实验题
实验室配制500mL0.2mol•L﹣1的FeSO4溶液,具体操作步骤为:
①在天平上称取一定质量的绿矾(FeSO4•7H2O),把它放在烧杯中,用适量的蒸馏水使其完全溶解;
②把制得的溶液小心的注入500mL的容量瓶中;
③继续向容量瓶中滴加蒸馏水至液面距刻度线1~2cm处时,改用胶头滴管小心滴加,直到溶液的凹液面恰好与刻度线相切为止;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次的洗涤液都转入容量瓶中,并轻轻摇匀;
⑤将容量瓶塞好,充分摇匀。
请填写下列空白.
(1)用托盘天平称取的绿矾的质量为: ;
(2)上述操作的正确顺序为: ;
(3)本次实验过程中多次用到玻璃棒,在溶解时玻璃棒的作用是: ,在移液时玻璃棒的作用是: .
(4)观察液面时,若俯视刻度线,会使所配制的溶液的浓度 (填“偏高”、“偏低”或“无影响”下同);加蒸馏水时不慎超过了刻度线后倒出部分溶液,使液面与刻度线相切,会 ;
(5)用ρ=1.84g•mL﹣1,质量分数为98%的浓硫酸配制200mL1mol•L﹣1的稀硫酸与上述配制溶液的步骤上的差别主要有三点:
①计算:理论上应取浓硫酸的体积V= mL(精确到小数点后两位);
②量取:由于量筒是一种粗略的量具,如想精确量取,必需选用 (填仪器名称).
③溶【解析】
稀释浓硫酸的方法 .
查看答案和解析>>
科目: 来源:2016届山东省青岛市高三上学期10月月考化学试卷(解析版) 题型:推断题
由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。
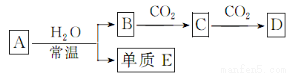
(1)若A为金属钠,则E为 ,A与水反应的离子方程式为 。
(2)若A为过氧化钠,则E为 ,A与水反应的化学方程式为 。
(3)A不论是Na还是Na2O2,依据转化关系判断物质D是 ,
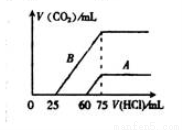
(4)向10ml某浓度的B溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况(不计CO2的溶解),则曲线B表明M中的溶质为 ;原NaOH溶液的物质的量浓度为 ;由曲线A、B可知,两次实验通入的CO2的体积比为 。
查看答案和解析>>
科目: 来源:2015-2016学年福建省高二上学期半期考试化学试卷(解析版) 题型:选择题
下列推论正确的是
A.S(g)+O2(g)===SO2(g) ΔH1;S(s)+O2===SO2(g) ΔH2,则ΔH1>ΔH2
B.C(石墨,s)===C(金刚石,s) ΔH=+1.9kJ·mol-1,则金刚石比石墨稳定
C.OH-(aq)+H+(aq)= H2O(l) ΔH=-57.4kJ·mol-1,则:含20gNaOH的稀溶液与过量稀醋酸完全反应,放出的热量为28.7kJ
D.2C(s)+O2(g)===2CO(g) ΔH=-221kJ·mol-1,则碳的燃烧热大于110.5kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com