
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中.然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.由此可见
A.NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH4HCO3+HCl→NH4Cl+CO2↑+H2O;△H<0
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是
A.加入10mL 0.01mol·L-1的NaOH溶液
B.加入10mL 0.01mol·L-1的盐酸溶液
C.加水稀释成100mL
D.加入10mL 的水进行稀释
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.25℃时,pH=3的1.0 L NaHSO3溶液中,含Na+数目为0.001NA
B.常温下,1L pH=12的Ba(OH)2 溶液中含OH—的数目为2NA
C.1L0.1mol·L—1的氨水中含有的NH3分子数小于0.1 NA
D.在高温高压下,28 gN2和6g H2充分反应生成NH3的分子数为2NA
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
在容积相同的两个密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol HI(a>b),可逆反应2HI  H2+I2(g)达到平衡后,下列说法正确的是
H2+I2(g)达到平衡后,下列说法正确的是
A.开始时A容器中的反应速率大于B容器中的反应速率
B.平衡时c(I2)A=c(I2)B
C. HI的平衡分解率:αA>αB
D.平衡时,I2蒸气在混合气体中的体积分数:A容器>B容器
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
已知:2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g)△H=﹣226kJ/mol
O2(g)△H=﹣226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为283 kJ
B.如图可表示由CO生成CO2的反应过程和能量关系

C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>﹣452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
相同温度、相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g) 3W(g)+2Z(g) △H=-Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如下表:
3W(g)+2Z(g) △H=-Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如下表:
X | Y | W | Z | 反应体系能量变化 | |
甲 | 2mol | 1mol | 放出a kJ/mol | ||
乙 | 1mol | 1mol | 放出b kJ/mol | ||
丙 | 2mol | 2mol | 放出c kJ/mol | ||
丁 | 3mol | 2mol | 吸收d kJ/mol |
下列说法正确的是
A.c+d<Q
B.平衡时,甲、丁容器中X、W的转化率之和等于1
C.平衡时丙容器中Z的物质的量浓度最大
D.X的转化率为:甲<乙<丙
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
一定温度时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应:PCl5(g)?Cl2(g)
+PCl3(g)经一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
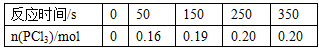
下列说法正确的是
A.反应在前50 s内的平均速率为v(PCl3)=0.0032 moI·L-l·s-l
B.保持其他条件不变,若升高温度,反应重新达到平衡,平衡时c(PCl3)=0.11moI·L-l, 则正反应的△H<0
C.相同温度下,若起始时向容器中充入1.0 molPCl5、0.20mol PCl3和0.20 mol Cl2,则反应达到平衡前v(正)<v(逆)
D.相同温度下,若起始时向容器中充入1.0mol PCl3、1.0 mol Cl2,则反应达到平衡时PCl3的转化率为80%
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:填空题
(10分)研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义。
(1) I2O5可使H2S、CO、HCl等氧化,常用于定量测定CO的含量。已知:
2I2(s)+5O2(g) 2I2O5(s) ΔH=-75.56 kJ·mol-1
2I2O5(s) ΔH=-75.56 kJ·mol-1
2CO(g)+O2(g) 2CO2(g) ΔH=-566.0 kJ·mol-1
2CO2(g) ΔH=-566.0 kJ·mol-1
写出CO(g)与I2O5(s)反应生成I2(s)和CO2(g)的热化学方程式: 。
(2) 降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0
N2(g)+2CO2(g) ΔH<0
①该反应的化学平衡常数表达式为K= 。
②一定条件下,将体积比为1∶2的NO、CO气体置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 (填字母)。
a. 体系压强保持不变
b. 混合气体颜色保持不变
c. N2和CO2的体积比保持不变
d. 每生成1 mol N2的同时生成2 mol NO
③若在一定温度下,将2 mol NO、1 mol CO充入1 L固定容积的容器中, 反应过程中各物质的浓度变化如下图所示。若保持温度不变,20 min时再向 容器中充入CO、N2各0.6 mol,平衡将 (填“向左”、“向右”或“不”)移动。20 min时,若改变反应条件,导致N2浓度发生如右图所示的变化,则改变的条件可能是 (填字母)。a. 加入催化剂 b. 降低温度 c. 增加CO2的量

查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:填空题
(16分)中学化学实验,淡黄色的pH试纸常用于测定溶液的酸碱性。在 25 ℃,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在如下平衡H2O  H++OH- ΔH>0。现欲使平衡向右移动,且所得溶液呈中性,选择的方法是 (填字母)。
H++OH- ΔH>0。现欲使平衡向右移动,且所得溶液呈中性,选择的方法是 (填字母)。
A.向水中加入NaHSO4溶液
B.向水中加入Cu(OH)2固体
C.加热水至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.在水中加入H2SO4溶液
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显 色,若用pH计测定,则pH 7 (填“>”“<”或“=”),溶液呈 性(填“酸”“碱”或“中”)。
(3)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5的酸碱性为 ,试样的pH= 。
(4)① 已知汽缸中生成NO的反应为N2(g)+O2(g) 2NO(g) ΔH>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
2NO(g) ΔH>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
② 汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的ΔH>0,简述该设想能否实现的依据 。
查看答案和解析>>
科目: 来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版) 题型:选择题
有人设想合成具有以下结构的烃分子,下列说法不正确的是

A.Ⅳ不可能合成得到
B.Ⅱ与苯互为同分异构体
C.Ⅲ(立方烷)的六氯代物共有3种
D.Ⅰ中各键之间夹角为109°28’
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com