
科目: 来源:2015-2016学年河北省高二上学期10月月考化学试卷(解析版) 题型:填空题
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放。在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),△H=-a kJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),△H=-a kJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
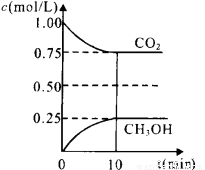
①能说明该反应已达平衡状态的是__________(填编号)
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O
D.该体系中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②计算该温度下此反应的平衡常数K=_________。(保留两位有效数字)。若改变条件 (填选项),可使K=1。
A.增大压强
B.增大反应物浓度
C.降低温度
D.升高温度
E.加入催化剂
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上学期10月月考化学试卷(解析版) 题型:填空题
工业上可以利用废气中的CO2为原料制取甲醇,其反应方程式为:CO2+3H2 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:
(1)已知常温常压下下列反应的能量变化如下图所示:

写出由二氧化碳和氢气制备甲醇的热化学方程式__ ,该反应的△S____________0(填“>”或“<”或“=”),在_______________情况下有利于该反应自发进行。
(2)如果上述反应方程式的平衡常数K值变大,则该反应__ (选填编号)。
A.一定向正反应方向移动
B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动
D.在平衡移动时逆反应速率先减小后增大
(3)若反应的容器容积为2.0L,反应时间4.0 min,容器内氢气的质量减少了4.8g,在这段时间内CO2的平均反应速率为 。
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
分析下列反应,在任何温度下均能自发进行的是
A.2N2(g)+O2(g)===2N2O(g)ΔH=+163 kJ·mol-1
B.Ag(s)+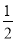 Cl2(g)===AgCl(s)ΔH=-127 kJ·mol-1
Cl2(g)===AgCl(s)ΔH=-127 kJ·mol-1
C.HgO(s)===Hg(l)+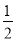 O2(g)ΔH=+91 kJ·mol-1
O2(g)ΔH=+91 kJ·mol-1
D.H2O2(l)=== 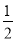 O2(g)+H2O(l)ΔH=-98 kJ·mol-1
O2(g)+H2O(l)ΔH=-98 kJ·mol-1
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
下列变化:①液态水汽化;②将胆矾加热变为白色粉末;③浓硫酸稀释;④氯酸钾分解;⑤生石灰跟水反应;属于吸热反应的是
A.②④ B.①④ C.②③ D.①④⑤
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
将BaO2放入密闭的真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
A.平衡常数减小 B.BaO量不变
C.氧气的浓度变小 D.BaO2量增加
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
在一定条件下,可逆反应X(g)十3Y(g) 2Z(g)达到平衡时,X的转化率与Y的转化率之比为1∶2,则起始充入容器中的X与Y的物质的量之比为
2Z(g)达到平衡时,X的转化率与Y的转化率之比为1∶2,则起始充入容器中的X与Y的物质的量之比为
A.1∶1 B.1∶3 C.2∶3 D.3∶2
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
下列说法中有明显错误的是
A.对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大
B.活化分子之间发生的碰撞一定为有效碰撞
C.升高温度,一般可使活化分子的百分数增大,因而反应速率增大
D.加适宜的催化剂,可使活化分子的百分数大大增加,从而增大反应速率
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
在密闭容器中发生反应:a A(g) c C(g)+d D(g),达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡浓度的1.8倍。下列叙述正确的是
c C(g)+d D(g),达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡浓度的1.8倍。下列叙述正确的是
A.A的转化率变大 B.平衡向正反应方向移动
C.D的体积分数变大 D.a<c+d
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:填空题
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
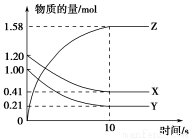
(1)反应开始到平衡,用Z表示的反应速率为 mol·L-1·s-1,Y的转化率 。
(2)该反应的化学方程式为 。
(3)10s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:
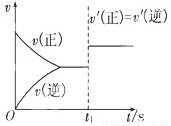
则下列说法符合该图像的是________________。
A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:填空题
合成氨工业的核心反应是N2(g)+3H2(g) 2NH3(g);反应过程中能量变化如图所示,回答下列问题。
2NH3(g);反应过程中能量变化如图所示,回答下列问题。
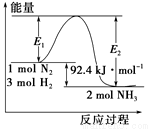
(1)该反应的ΔH=____________kJ/mol。
(2)在反应体系中加入催化剂,反应速率增大,E1的变化:E1__________(填“增大”、“减小”或“不变”)。
(3)在500℃、2×107Pa和催化剂条件下,向一密闭容器中充入0.5mol N2和1.5mol H2,充分反应后,放出的热量____________46.2 kJ (填“<”、“>”或“=”) 。
(4)关于该反应的下列说法中,正确的是________(填字母)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
(5)已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)===P4O10(s) ΔH 1=-2983.2 kJ·mol-1
P(s,红磷)+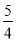 O2(g)===
O2(g)=== 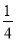 P4O10(s) ΔH 2=-738.5 kJ·mol-1
P4O10(s) ΔH 2=-738.5 kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com