
科目: 来源:2016届江苏省淮安市高三上学期9月月考化学试卷(解析版) 题型:填空题
(12分)结构决定性质,性质体现结构。对结构和性质的研究是学好化学的基础。
(1)N、O、S三种元素的第一电离能大小顺序为: > > 。(填元素符号)
(2)已知水的沸点远高于H2S,这是由于 。
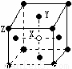
(3)某晶体的晶胞如右图所示,X位于体心,Y位于4个面心,Z位于8个顶点,该晶体中 X、Y、Z的粒子个数比为 。
(4)Cu2Cl2·2CO·2H2O是一种配合物,其结构如右图所示:
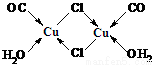
①与CO为互为等电子体的分子是 。
②该配合物中,氯离子的杂化方式为 ;
金属阳离子的核外电子排布式为 。
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上学期第一次月考化学试卷(解析版) 题型:选择题
在C(s)+CO2(g)?2CO(g)反应中可使反应速率增大的措施是
①缩小容器的体积;②增加碳的量;③通入CO2;④恒压下充入N2;⑤恒容下充入N2;⑥通入CO.
A.①③⑤ B.②④⑥ C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上学期第一次月考化学试卷(解析版) 题型:填空题
(14 分,每空 2 分)下表是稀硫酸与某金属反应的实验数据:
实验 | 金属 | 金属 | C(H2SO4) | V(H2SO4) | 溶液温度/℃ | 金属消失 | |
序号 | 质量/g | 状态 | /mol·L-1 | /mL | 反应前 | 反应后 | 的时间/s |
1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
分析上述数据,回答下列问题:
(1)实验 4 和 5 表明,___________对反应速率有影响,____________反应速率越快,能表明同一规律的实验还有____________(填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有 ____ (填实验序号);
(3)本实验中影响反应速率的其他因素还有 ________ ,其实验序号是 ____ 。
(4)实验中的所有反应,反应前后溶液的温度变化值(约 15℃)相近,推测其原因: 。
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上学期第一次月考化学试卷(解析版) 题型:填空题
(12分)有科学家正在研究用碳与一氧化氮反应处理环境问题:
C(s)+2NO(g)?CO2(g)+N2(g)△H
(1)实验方案中有下列措施①采用加热提高反应速率②使用催化剂提高反应速率③使用加压提高NO转化率④使CO2转化成干冰从体系用脱离,提高NO的转化率其中你认为可行的是 .(2分)
(2)这个反应的平衡常数表达式是 .(1分)
(3)在恒容恒温密闭容器中,科学家得到下列实验数据:
浓度(mol/L)
时间(min) NO N2 CO2
0 0.100 0 0
10 0.058 0.021 0.021
20 0.040 0.030 0.030
30 0.040 0.030 0.030
请求出该应在该温度下的平衡常数K= .(2分)
(4)若在(3)的实验中30min时开始升温,36min时达平衡,测得NO的转化率变为50%,则该反应的△H 0(1分)(填“>”、“<”、“=”),判断的理由是 .(2分)
(5)若科学家在30min后改变了某一条件,反应进行到40min时达平衡浓度分别为C(NO)=0.032mol/L,C(N2)=0.034mol/L,C(CO2)=0.017mol/L,则改变的条件可能是 ,(2分)判断的依据是 .(2分)
查看答案和解析>>
科目: 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子质量为32g
D.标准状况下,0.5 mol任何物质的体积均约为11.2L
查看答案和解析>>
科目: 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列关于仪器的识别中错误的是




A. 三脚架 B. 蒸发皿 C. 坩埚钳 D.泥三角
查看答案和解析>>
科目: 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤;正确的操作顺序是
A.③②①⑤④ B.①②③⑤④
C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目: 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
对于某些常见离子的检验及结论一定正确的是
A.加稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加氯化钡溶液有白色沉淀产生,再加盐酸沉淀不消失,一定有SO42-
C.加入氯化钠溶液有白色沉淀产生,再加稀硝酸沉淀不消失,一定有Ag+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目: 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:实验题
(10分)用质量分数为36.5%的盐酸(密度为1.16g•cm﹣3)配制1mol•L﹣1的稀盐酸.现实验室仅需要这种盐酸220mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为 mL的容量瓶。
(2)计算已知盐酸的物质的量浓度为 。
(3)经计算需要 mL浓盐酸,在量取时宜选用下列量筒中的 。
A.5mL B.10mL C.25mL D.50mL
(4)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号) 。
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是 (填“偏高”、“偏低”或“无影响”).若用干燥洁净的量筒量取浓盐酸时俯视,则配制的稀盐酸浓度是 (填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:填空题
(10分)将25℃ 101KPa条件下的氯化氢(HCl)气体49.6L,通入492mL水中,(已知水的密度为:1.00g/mL),得到密度为1.13g/mL的盐酸(即氯化氢的水溶液)。注:25℃101KPa条件下气体摩尔体积为24.8L/mol。
(1)此盐酸的质量分数为 (计算结果保留一位小数)
(2)此盐酸的物质的量浓度为 (计算结果保留一位小数)
(3)取出20.0 mL该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是 mL(计算结果保留一位小数)
(4)0.100 mol/L的稀盐酸500mL中含有的Cl-的数目为 (计算结果保留两位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com