
科目: 来源:2015-2016学年辽宁省高一上学期期中测试化学试卷(解析版) 题型:填空题
现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3·H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-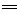 H2O,该反应的化学方程式为 。
H2O,该反应的化学方程式为 。
(2)⑩在水中的电离方程式为 ,
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式: ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:
(4)写出下列反应的离子方程式
向Ba(OH)2溶液中逐滴加入稀硫酸 。
向Ba(OH)2溶液中通入过量的CO2 。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:选择题
对已达化学平衡的下列反应 2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是:
2Z(g),减小压强时,对反应产生的影响是:
A、逆反应速率增大,正反应速率减小
B、逆反应速率减小,正反应速率增大
C、逆反应速率先增大后减小
D、正反应速率先减小后增大
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列关于反应能量的说法正确的是
A、101kPa时,H2(g)+1/2O2(g)===H2O(g) ΔH=-248kJ·mol-1,H2的燃烧热为248kJ·mol-1
B、利用盖斯定律可以计算难以测量的反应热
C、H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,含1 mol NaOH的氢氧化钠的溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量
D、相同条件下,如果1 mol H原子所具有的能量为E1,1 mol H2所具有能量为E2,则2E1=E2
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:选择题
将0.05molSO2(g)和0.03molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g)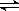 2SO3(g),在一定条件下2min时达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
2SO3(g),在一定条件下2min时达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
A、若恒容下,充入氮气,则c(SO3)小于0.04mol·L-1
B、该条件下反应的平衡常数为1.6×103
C、v(O2)= 0.02 mol·L-1.min-1
D、使用催化剂若平衡没有移动,则该反应达到化学平衡状态
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列叙述正确的是:
A、铜、铁和FeCl3溶液形成的原电池,铜极放出氢气
B、电解硫酸钠溶液就是电解水,电解后溶液pH升高
C、铁锅生锈的正极反应为:O2+2H2O+4e-===4OH-
D、工业上电解饱和食盐水的阳极反应为:2H++2e-===H2↑
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:选择题
已知有热化学方程式:SO2(g)+ 1/2 O2(g) = SO3(g);△H =-98.32kJ/mol。现有2molSO2参加反应,当放出137.5kJ热量时,SO2的转化率最接近于
A、40% B、50% C、70% D、90%
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:填空题
(15分)按要求回答下列问题
(1)、4g CO在氧气中燃烧生成CO2,放出 9. 6kJ热量,写出CO燃烧的热化学方程式。_____________________________
(2)、已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为________________________
(3)、已知碳的燃烧热ΔH1= a kJ·mol-1 S(s)+2K(s)==K2S(s) ΔH2= b kJ·mol-1
2K(s)+N2(g)+3O2(g)==2KNO3(s) ΔH3= c kJ·mol-1
则S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g) ΔH=
(4)、已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol一1
H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ·mol一1
CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ·mol一1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式
计算10m3(标况)水煤气完全燃烧放出的热量为 kJ(结果保留到小数点后一位)。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上学期期中测试化学试卷(解析版) 题型:填空题
(10分)高炉炼铁过程中发生的主要反应为:1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的平衡常数表达式K=________ ,ΔH________0(填“>”、“<”或“=”);
(2)在一个容积为5L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时比较v(正) v(逆) (填“>” “=” “<”),反应经过2min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=________ ,CO的平衡转化率=________ ;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________。
A、减少Fe的量 B、增加Fe2O3的量 C、移出部分CO2
D、提高反应温度 E、减小容器的容积 F、加入合适的催化剂
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高一上学期期中测试化学试卷(解析版) 题型:选择题
科学的分类方法可提高学习效率,以达到事半功倍的效果。下列分类标准合理的是
①根据氧化物的元素组成将氧化物分为金属氧化物和非金属氧化物;
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应;
③根据分散系是否有丁达尔效应来区分溶液、胶体;
④根据在水溶液里或者熔融状态下能否导电可将纯净物分为电解质和非电解质.
A.①②④ B.①②③ C.②③④ D.全部
查看答案和解析>>
科目: 来源:2015-2016学年湖南省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列变化需要加入还原剂才能实现的
A.MnO4- Mn2+ B.HCl
Mn2+ B.HCl Cl2
Cl2
C.Fe Fe3+ D.KClO3
Fe3+ D.KClO3 O2
O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com