
科目: 来源:2016届江苏省淮安市高三上学期11月月考化学试卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的的是
A.制备Al(OH)3悬浊液:向1mol·L-1AlCl3溶液中加过量的6mol·L-1NaOH溶液
B.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和氢氧化钠溶液,振荡后静置分液,并除去有机相的水
C.检验溶液中是否含有Fe2+:取少量待检验溶液,向其中滴加KSCN溶液,再加入少量新制氯水,观察实验现象
D.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象
查看答案和解析>>
科目: 来源:2016届江苏省淮安市高三上学期11月月考化学试卷(解析版) 题型:填空题
利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:
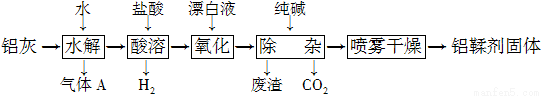
(1) 气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为____________。“水解”采用90 ℃而不在室温下进行的原因是___________________。
(2) “酸溶”时,Al2O3发生反应的离子方程式为 。
(3) “氧化”时,发生反应的离子方程式为 。
(4) “废渣”成分为______________(填化学式)。
(5) 采用喷雾干燥而不用蒸发的原因是 。
查看答案和解析>>
科目: 来源:2016届江苏省淮安市高三上学期11月月考化学试卷(解析版) 题型:填空题
Ⅰ.甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是CO(g)+2H2(g)===CH3OH(g) ΔH=-90.8 kJ·mol-1。
已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
①H2的燃烧热ΔH=___________kJ·mol-1。
②CH3OH(g)+O2(g)===CO(g)+2H2O(g)的反应热ΔH=________________。
(2)工业上利用甲醇制备氢气常用方法之一是甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)===CO(g)+2H2(g),此反应能自发进行的原因是____________________________。
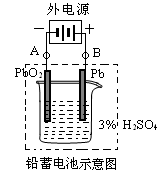
Ⅱ.铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是________________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
(2)在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成________、B电极上生成________。
查看答案和解析>>
科目: 来源:2016届湖北省枣阳市高三上学期10月月考理综化学试卷(解析版) 题型:选择题
下列说法错误的是
A.第ⅤA族元素的几种气态氢化物中,NH3是稳定性最高的氢化物
B.由于C22—和O22+为等电子体,所以可以判断O22+的电子式为
C.含离子键的纯净物一定存在金属元素
D.某反应X(g)+Y(g)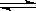 Z(g) △H<0 分两步进行:X(g)+Y(g)
Z(g) △H<0 分两步进行:X(g)+Y(g)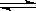 W(g) △H>0和W(g)
W(g) △H>0和W(g)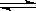 Z(g) △H<0,反应过程中的能量变化如右图:
Z(g) △H<0,反应过程中的能量变化如右图:

查看答案和解析>>
科目: 来源:2016届湖北省枣阳市高三上学期10月月考理综化学试卷(解析版) 题型:选择题
分子式与苯丙氨酸( )相同,且同时符合下列两个条件:①有带两个取代基的苯环 ②有一个硝基直接连接在苯环上的异构体的数目是
)相同,且同时符合下列两个条件:①有带两个取代基的苯环 ②有一个硝基直接连接在苯环上的异构体的数目是
A.3 B.5 C.6 D.10
查看答案和解析>>
科目: 来源:2016届湖北省枣阳市高三上学期10月月考理综化学试卷(解析版) 题型:填空题
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)的工艺流程如下:
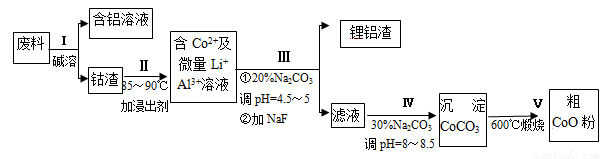
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 。
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为(产物中无沉淀且只有一种酸根) 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因______________ 。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式____________________。
(4)碳酸钠溶液在过程Ⅲ和Ⅳ中所起作用有所不同,请写出在过程IV中起的作用是_____________。
(5)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是____________(填序号)。
A. c(Na+) = 2c(CO32-)
B.c(Na+) > c(CO32-) > c(HCO3-)
C. c(OH-) > c(HCO3-) > c(H+)
D. c(OH-) - c(H+) == c(HCO3-) + 2c(H2CO3)
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。下图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,A物质的化学式是____________。

查看答案和解析>>
科目: 来源:2016届湖北省襄阳市高三上学期期中测试化学试卷(解析版) 题型:选择题
下图所示装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色。下列说法正确的是
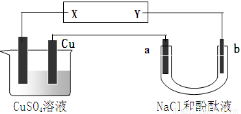
A.NaCl溶液浓度不变 B.X是负极,Y是正极
C.CuSO4溶液浓度变小 D.X是正极,Y是负极
查看答案和解析>>
科目: 来源:2016届湖北省襄阳市高三上学期期中测试化学试卷(解析版) 题型:选择题
用NA表示的值。下列叙述正确的是
A.17g羟基(-OH)所含有的电子数是10 NA个
B.1mol苯乙烯中含有的碳、碳双键数为4NA个
C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个
D.4.2g C3H6中含有的碳碳双键数一定为0.1NA
查看答案和解析>>
科目: 来源:2016届湖北省襄阳市高三上学期期中测试化学试卷(解析版) 题型:选择题
工业上常用还原沉淀法处理含铬废水(Cr2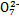 和Cr
和Cr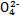 ),其流为:
),其流为:
Cr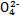
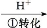 Cr2
Cr2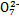
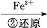 Cr3+
Cr3+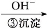 Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr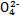 (黄色)+2H+
(黄色)+2H+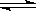 Cr2
Cr2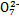 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) 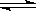 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr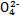 浓度增大
浓度增大
B.步骤①中当2v(Cr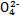 )=v(Cr2
)=v(Cr2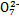 )时,说明反应2Cr
)时,说明反应2Cr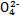 (黄色)+2H+
(黄色)+2H+  Cr2
Cr2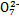 (橙色)+H2O达到平衡状态
(橙色)+H2O达到平衡状态
C.步骤②中,若要还原1 mol Cr2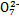 ,需要12 mol (NH4)2Fe(SO4)2·6H2O
,需要12 mol (NH4)2Fe(SO4)2·6H2O
D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com