
科目: 来源:2015-2016学年江苏省高一上期中测试化学试卷(解析版) 题型:填空题
(12分)已知实验室制取C12的反应为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,又已知Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,也能氧化浓盐酸生成C12;
MnCl2+Cl2↑+2H2O,又已知Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,也能氧化浓盐酸生成C12;
(1)写出PbO2与浓盐酸反应的化学方程式 ,其中表现还原性的HCl与表现酸性的HCl的物质的量之比为 。
(2)PbO2不稳定,随温度升高按下列顺序逐步分【解析】
PbO2→Pb2O3→Pb3O4→PbO。若加热分解后所得到的固体全部为Pb3O4,现将a molPbO2加热分解,则加热过程中放出O2__ ___L(标准状况下);
(3)已知PbSO4不溶于水,但可溶于醋酸铵溶液,反应方程式如下:PbSO4+2CH3COONH4= (CH3COO)2Pb+(NH4)2SO4。
①PbSO4与CH3COONH4能进行反应的原因是符合了复分解反应条件之一的生成了 ,现将Na2S溶液与醋酸铅溶液混合有沉淀生成,则其反应的离子方程式应为 。
②已知+2价Sn的化合物具有强还原性。等物质的量的PbO2和SnO的混合物溶于过量的稀硫酸中,溶液中存在的主要金属阳离子是 (填序号)。
A.Pb2+ B.Pb4+ C.Sn2+ D.Sn4+
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
下列事实不能用勒沙特列原理解释的是:
A.新制的氯水在光照条件下颜色变浅
B.加入催化剂可以加快合成氨的速率
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
A.强酸溶液产生较多的氢气 B.两者产生等量的氢气
C.无法比较两者产生氢气的量 D.弱酸溶液产生较多的氢气
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
用水稀释0.1mol·L-1氨水时,溶液中随着水量的增加而减小的是
A.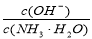
B.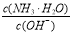
C.c(H+)和c(OH-)的乘积
D.OH-的物质的量
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:选择题
在密闭容器中,反应2HI H2+I2 △H > 0,当达到平衡时,欲使混合气体颜色加深,可采取的措施有
H2+I2 △H > 0,当达到平衡时,欲使混合气体颜色加深,可采取的措施有
A.减小容器体积 B.降低温度
C.加入催化剂 D.恒容下充入HI气体
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:实验题
(16分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计] 控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验:
(1)请完成以下实验设计表(表中不要留空格)
实验编号 | 实验目的 | T/K | pH | c/10-3 mol·L-1 | |
H2O2 | Fe2+ | ||||
① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
② | 探究温度对降解反应速率的影响 | 3 | |||
③ | 298 | 10 | 6.0 | 0.30 | |
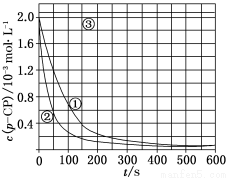
[数据处理] 实验测得p-CP的浓度随时间变化的关系如上图
(2)请根据上图实验①曲线,计算降解反应50~150 s内的反应速率:v(p-CP)=__ _____mol·L-1·s-1;
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但后续研究表明:温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:_____________;
(4)实验③得出的结论是:pH等于10时,反应 (填“能”或“不能”)进行;
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法: 。
查看答案和解析>>
科目: 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:填空题
(18分)合成氨是人类科学技术上的一项重大突破。工业上以天然气为原料合成氨。其生产工艺如下:造气阶段→转化阶段→分离净化→合成阶段
(1)造气阶段的反应为:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.1 kJ/mol
CO(g)+3H2(g) ΔH=+206.1 kJ/mol
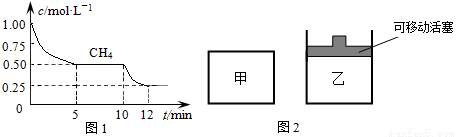
①在一密闭容器中进行上述反应,测得 CH4的物质的量浓度随反应时间的变化如下图1所示。反应中处于平衡状态的时间为 、 ;10 min时,改变的外界条件可能是 。
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O。在相同温度下发生反应,并维持反应过程中温度不变。则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4) α乙(CH4);
(2)转化阶段发生的可逆反应为: CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
一定温度下,反应的平衡常数为K=1。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO | H2O | CO2 | H2 |
0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应中正、逆反应速率的关系式是 (填序号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)  2NH3(g) ∆H=-92.4kJ•mol ?1
2NH3(g) ∆H=-92.4kJ•mol ?1
①依据温度对合成氨反应的影响,在下图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。
②根据勒夏特列原理,简述提高合成氨原料转化率的一种方法 。

(4)工业合成氨的热化学方程式为
N2(g)+3H2(g)  2NH3(g),ΔH=-92.4 kJ·mol-1。
2NH3(g),ΔH=-92.4 kJ·mol-1。
在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。求:
①该条件下的平衡常数为_________;
②若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。反应放出的热量________(填“>”“<”或“=”)92.4 kJ。
查看答案和解析>>
科目: 来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列说法正确的是
A.14g聚乙烯中所含原子数为3NA
B.48g甲硫醇(CH4S)中含有C—H键数目为4NA
C.标准状况下,11.2L氯仿所含分子数为0.5NA
D.0.1mol苯乙烯中含有双键的数目为0.4NA
查看答案和解析>>
科目: 来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版) 题型:选择题
用2-丁炔为原料制取CH3CHBrCBrClCH3,可行的反应途径是
A.先加Cl2,再加Br2 B.先加Cl2,再加HBr
C.先加HCl,再加HBr D.先加HCl,再加Br2
查看答案和解析>>
科目: 来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版) 题型:选择题
已知: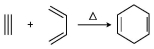 。若要合成
。若要合成 ,则所用的反应物可以是
,则所用的反应物可以是
①2-甲基-1,3-丁二烯和2-丁炔 ②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔 ④2,3-二甲基-1,3-丁二烯和丙炔
A.①④ B. ①② C.②④ D. ②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com