
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:推断题
[化学——选修5:有机化学基础](14分)
A(C2H2)是基本有机化工原料。由A制备聚乙烯醇缩丁醛和顺式异戊二烯的合成路线(部分反应条件略去)如图所示:

回答下列问题:
(1)A的名称是 ,B含有的官能团是 。
(2)①的反应类型是 ,⑦的反应类型是 。
(3)C、D的结构简式分别为 。
(4)3-氯-3-甲基-1-丁烯一定条件下,也可以反应得到异戊二烯,请写出反应方程式(注明条件)_________________________
(5)写出与A具有相同官能团的异戊二烯的所有同分异构体 (写结构简式)。
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.Fe与S混合加热生成FeS2
B.Fe(OH)3胶体无色、透明,能发生丁达尔现象
C.H2、SO2、CO2三种气体都可用浓硫酸干燥
D.SiO2既能和氢氧化钠溶液反应,也能和氢氟酸反应,所以是两性氧化物
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A.热的浓盐酸可以除去烧瓶内残留的MnO2
B.过量的铜与浓硝酸反应会有一氧化氮生成
C.稀硝酸可除去试管内壁的银镜
D.白磷在空气中加热到一定温度能转化成红磷
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
下列关于物质或离子检验的叙述正确的是
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
下列各选项中,不能利用置换反应通过Y得到W的一组化合物是
选项 化合物 | A | B | C | D |
Y | CO2 | Fe2O3 | H2O | FeCl3 |
W | MgO | Al2O3 | HF | CuCl2 |
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
高铁酸钾(K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.常温下浓硫酸能和铝发生钝化,可在常温下用铝制容器贮运浓硫酸
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.二氧化氯具有还原性,可用于自来水的杀菌消毒
D.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
120mL含有0.20mol碳酸钠溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
A.2.0mol/L B.1.5 mol/L C.0.18 mol/L D.0.24mol/L
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:选择题
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如何利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).
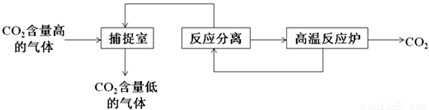
下列有关该方法的叙述中正确的是
A.能耗大是该方法的一大缺点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
D.该方法可减少碳排放,捕捉到的CO2还可用来制备尿素等产品
查看答案和解析>>
科目: 来源:2016届江苏省高三上学期9月学情调研化学试卷(解析版) 题型:填空题
磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图_____________________。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500°C生成白磷,反应为:
2Ca3(PO4)2+6SiO2==6CaSiO3+P4O10 10C+P4O10==P4+10CO
每生成 1molP4 时,就有 mol电子发生转移。
(3)硫代硫酸钠(Na2S2O2)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素完全氧化,剩余的I2 用Na2S2O2溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入amolL-1I2溶液V1ml,充分反应后,用Na2S2O2溶液滴定剩余的I2,消耗bmolL-1 Na2S2O2溶液V2ml.该溶液中维生素C的物质量是 mol。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生反应,生成物之一可以用淀粉溶液检验。根据反应溶液出现蓝色所需的时间来衡量该反应的速率,写出该反应的离子方程式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com