
科目: 来源:2015-2016学年四川省高二10月月考化学试卷(解析版) 题型:选择题
等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)  2Z(g)+W(s)ΔH<0,下列叙述正确的是( )
2Z(g)+W(s)ΔH<0,下列叙述正确的是( )
A.平衡常数K值越大,X的转化率越大
B.达到平衡时,反应速率v正(X)=2v逆(Z)
C.达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二10月月考化学试卷(解析版) 题型:选择题
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知
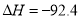 kJ·mol
kJ·mol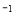 )
)
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol·L | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 |
|
|
|
下列说法正确的是
A.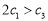 B.α1+α3=1 C.
B.α1+α3=1 C.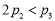 D.
D.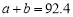
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二10月月考化学试卷(解析版) 题型:填空题
(13分)在固定容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g)随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g)随温度升高,混合气体的颜色变深。回答下列问题:
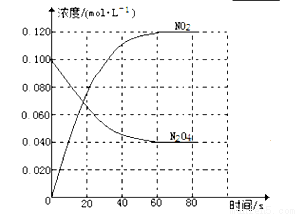
(1)反应的△H 0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为 。 反应的平衡常数K1= 。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)降低,经10s又达到平衡。
①T 100℃(填“大于”“小于”),判断理由是 。
②100℃时达到平衡后,向容器中再充入0.20mol NO2气体,新平衡建立后,NO2的体积分数
(填“增大”、“不变”或“减小”)
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反应”)方向移动,判断理由是 。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二10月月考化学试卷(解析版) 题型:填空题
( 16分)一定温度下,将3 molA气体和1 molB气体通入一密闭容器中,发生如下反应:3A(g)+B(g)  xC(g),请填写下列空白:
xC(g),请填写下列空白:
(1)若容器体积固定为 2 L,反应1 min 时测得剩余1.8 mol A,C的浓度为0.4 mol/L。
①1 min内,B的平均反应速率为__ ______;x为________。
②若反应经2 min达到平衡,平衡时C的浓度________0.8 mol/L(填“大于”、“等于”、“小于”)
③平衡混合物中,C的体积分数为22%,则A的转化率是____ ____。
④改变起始物质加入的量,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的量n(A)、n(B)、n(C)之间应满足的关系式:______ ______。
(2)若维持容器压强不变
①达到平衡时C的体积分数________22%,(填“大于”、“等于”、“小于”);
②改变起始物质加入的量,欲使反应达到平衡时C的物质的量是原平衡的2 倍,则应加入________mol A气体和 ________mol B气体。
查看答案和解析>>
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.0.1mol/L NaOH溶液中,Na+个数为0.1NA
B.Na2O2与足量的水反应生成1molO2,转移电子数目为2NA
C.2 L0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2 NA
D.1molO2和O3混合气体中含有氧原子的数目为2.5NA
查看答案和解析>>
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:选择题
常温下,水溶液中能大量共存的一组离子是
A.与Al反应放出氢气的溶液中:Na+、H+、NH4+、NO3—
B.在c(H+)=1.0×10—13mol/L的溶液中:Na+、K+、AlO2—、CO32—
C.澄清透明的溶液中:Fe3+、Mg2+、NO3—、S2—
D.在pH=1的溶液中:NH4+、K+、ClO—、Cl—
查看答案和解析>>
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:选择题
表中陈述I、II均正确,且两者在反应原理上相似的是
选项 | 陈述I | 陈述II |
A | 向酚酞溶液中加Na2O2,溶液先变红后褪色 | 向石蕊溶液中通入SO2,溶液先变红后褪色 |
B | 将SO2和Cl2同时通入BaCl2溶液中,产生白色沉淀 | 将CO2和NH3同时通入CaCl2溶液中,产生白色沉淀 |
C | 向MgCl2溶液中加入NaOH溶液生成白色沉淀 | 向FeCl3溶液中加入NaOH溶液生成红褐色沉淀 |
D | Na投入水中产生大量气泡 | Na2CO3投入盐酸中产生大量气泡 |
查看答案和解析>>
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:选择题
向30mL 1mol/L的AlCl3溶液中逐渐加入浓度为4mol/L的NaOH溶液,若产生0.78g白色沉淀,则加入的NaOH溶液的体积可能为
A.3mL B.7.5mL C.15mL D.17.5mL
查看答案和解析>>
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:实验题
(15分)钢铁企业酸洗钢材时产生的废液主要成分为Fe2+、H+、Cl-,可用下述方法处理该废液,回收盐酸和制备氧化铁涂料。
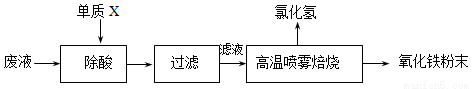
(1)单质X的化学式是 。
(2)氯化亚铁溶液经高温喷雾焙烧转化为HCl气体和氧化铁粉末,有关的化学方程式依次为: 。
(3)某铁红涂料中除含有Fe2O3外,还可能添加有CuO或FeO中的一种,请设计实验方案,探究该铁红涂料中添加物的成分。
① 提出合理假设
假设1:添加了CuO
假设2:添加了FeO
② 请设计方案,验证上述假设,写出实验步骤、预期现象和结论。
限选试剂:铁粉、3mol•L-1H2SO4、0.1 mol•L-1酸性KMnO4溶液、10%NaOH溶液、10%H2O2、KSCN溶液
操作步骤 | 预期现象和结论 |
步骤1.取少量样品于试管中, ____________________________ | 样品全部溶解,得到澄清的溶液。 |
步骤2. __________________ 步骤3. __________________ | ___________________________ ___________________________ ___________________________ ___________________________ |
(4)请计算,用635g水完全吸收“高温喷雾焙烧”产生的HCl气体 升(标准状况),即可得到36.5%的浓盐酸(相对原子质量 Cl 35.5 H 1)。
查看答案和解析>>
科目: 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:填空题
[化学——选修2:化学与技术](14分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系, 在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
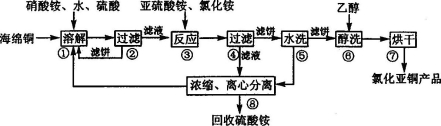
回答下列问题:
(1)步骤①中得到的氧化产物是 。溶解温度应控制在60~70℃,原因是 。
(2)写出步骤③中主要反应的离子方程式 。
(3)步骤⑤包括用pH = 2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是 。
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有 (填字母)。
A.分馏塔 8.离心机 C.反应釜 D.框式压滤机
(6)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+。样品中CuCl的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com